乳がんのゲノム医療
乳がんのゲノム医療:個別化治療への進化
ゲノム医療は、乳がん治療において革新的な進展を遂げています。ゲノム医療とは、がん細胞の遺伝的変異や分子プロファイルを解析し、それに基づいて最適な治療法を選択する個別化医療です。特に乳がんにおいては、がんの分子プロファイルに基づいて治療が最適化されることにより、患者ごとの治療効果を高め、副作用を最小限に抑えることが期待されています。ここでは、乳がんのゲノム医療の最新の進展と、それがどのように治療に役立っているかを詳細にまとめます。
1. ゲノム医療の基本概念
ゲノム医療は、患者個々のがん細胞の遺伝子変異や分子標的を解析し、それに基づいた治療を行うアプローチです。乳がんは遺伝的に多様な疾患であり、腫瘍の特性に応じて治療法が異なるため、従来の画一的な治療では限界がありました。しかし、次世代シーケンシング(NGS)技術の進化により、がん細胞の遺伝的特徴を迅速に解明することが可能となり、個別化された治療が実現しています。
2. 乳がんにおける主要な遺伝子変異とその影響
乳がんでは、いくつかの主要な遺伝子変異が治療の選択に大きな影響を与えます。これらの変異は、乳がんの発生や進展に関与しており、これらを標的とした治療が開発されています。
2.1 BRCA1/BRCA2変異
BRCA1およびBRCA2遺伝子の変異は、乳がんのリスクを大幅に増加させることが知られています。これらの遺伝子はDNA修復に関与しており、変異があるとDNA修復機能が損なわれ、がんの発生リスクが高まります。この遺伝子変異を持つ乳がん患者に対しては、PARP阻害薬が有効であることが示されています。PARP阻害薬は、がん細胞がDNA修復を行う経路をさらに遮断し、がん細胞の死滅を促進します。
2.2 PIK3CA変異
PIK3CA遺伝子の変異は、ホルモン受容体陽性(ER+)の乳がん患者において高頻度で発見されます。この変異は、PI3K経路を活性化させ、がん細胞の成長や生存を促進します。PIK3CA変異を持つ患者に対しては、アルペリシブ(Alpelisib)などのPI3K阻害薬が使用されており、治療効果が示されています。
2.3 ESR1変異
ホルモン療法に対する耐性の発現に関与する遺伝子変異として、ESR1遺伝子の変異が知られています。この変異は、ホルモン受容体の活性化を促進し、ホルモン療法への抵抗性を引き起こすことがあります。このような耐性を克服するために、ホルモン療法と分子標的薬の併用が検討されており、特にCDK4/6阻害薬が有効な治療法として使用されています。
3. ゲノム医療とバイオマーカーの活用
ゲノム医療において、バイオマーカーは治療法を選択する際に重要な役割を果たします。バイオマーカーは、がんの進行や治療に対する反応を予測する指標として使用され、特定のバイオマーカーに基づいて最適な治療法を選択することができます。
3.1 HER2
HER2は乳がんの治療における最もよく知られたバイオマーカーの一つです。HER2が過剰に発現している乳がん患者には、トラスツズマブ(ハーセプチン)やペルツズマブなどの抗HER2治療が効果的です。最近の研究では、HER2の発現が非常に低い「HER2ウルトラロー」と呼ばれる患者に対しても、抗HER2治療が有効であることが示されており、治療の幅が広がっています。
3.2 PD-L1と免疫療法
PD-L1は、がん細胞が免疫細胞による攻撃を回避するために発現させるタンパク質であり、免疫チェックポイント阻害薬のターゲットとなります。PD-L1が高発現している乳がん患者に対しては、ペンブロリズマブ(Keytruda)などの免疫療法が有効であることが示されており、特にトリプルネガティブ乳がん(TNBC)において顕著な治療効果を発揮しています。
3.3 液体生検と循環腫瘍DNA(ctDNA)
液体生検は、血液中の循環腫瘍DNA(ctDNA)を検出し、がんの遺伝的変異をリアルタイムで監視する手法です。液体生検は、がんの進行や再発を早期に発見し、治療効果をモニタリングするために使用されています。これにより、治療を迅速に調整し、個別化治療の精度が向上することが期待されています。
4. ゲノム医療の課題と将来の展望
ゲノム医療は乳がん治療において多大な可能性を秘めていますが、いくつかの課題も存在します。まず、遺伝子変異に基づいた治療法の選択には、十分な臨床データの蓄積が必要です。また、すべての患者が遺伝子解析を受けられるわけではなく、経済的・地域的な格差が存在します。
さらに、ゲノム解析の結果に基づいて選択される治療法の効果は、すべての患者で同様に高いわけではありません。がんの進行状態や遺伝子変異の種類に応じて、治療効果が異なるため、今後はより精度の高いバイオマーカーの開発が求められます。
一方で、ゲノム医療の未来は非常に明るく、以下のような新しい技術やアプローチが進行中です。
- 人工知能(AI)の活用:AIを用いたゲノムデータ解析により、がんの進行を予測し、最適な治療法を提案する技術が進化しています。これにより、治療の個別化がさらに進むことが期待されています。
- 新しいバイオマーカーの発見:次世代シーケンシング技術の進展により、がんの進行や治療に関連する新しいバイオマーカーが次々と発見されています。これにより、より多くの患者が個別化治療の恩恵を受けることが可能となります。
まとめ
乳がんのゲノム医療は、個別化治療の実現に向けた重要な要素となっています。BRCA1/BRCA2やPIK3CA、ESR1などの遺伝子変異に基づいた治療法が開発され、治療の選択肢が広がっています。さらに、液体生検や循環腫瘍DNA(ctDNA)の活用により、治療効果をモまとめた内容は以下の通りです。
乳がんのゲノム医療は、患者個々のがん細胞の遺伝的変異や分子プロファイルを基に、個別化治療を行う最新のアプローチです。この方法では、BRCA1/BRCA2遺伝子変異やPIK3CA遺伝子変異など、乳がんの発症や進展に関与する特定の遺伝子を解析し、それに基づいた治療が選択されます。特に、次世代シーケンシング(NGS)技術の進展により、患者ごとの遺伝的特性を詳細に解析することが可能となり、これに基づいて個別化治療が実現しています。
また、治療の選択肢をさらに広げるために、バイオマーカーが治療戦略の中で重要な役割を果たしています。HER2、PD-L1、ESR1などのバイオマーカーは、乳がんのサブタイプや治療に対する反応を予測するために使用され、特定の治療法がどの患者に最も効果的かを判断するための指標となります。
さらに、液体生検や循環腫瘍DNA(ctDNA)を活用することで、がんの進行や再発を早期に発見し、治療効果をモニタリングすることが可能となり、治療の個別化がより正確に行われるようになっています。これらの技術は、特に再発リスクの高い乳がん患者の治療において効果を発揮しています。
将来の課題としては、すべての患者がこの高度な医療にアクセスできるわけではないことや、遺伝的解析の結果がすべての患者において有効とは限らないことが挙げられます。しかし、人工知能(AI)を用いた解析技術の進展や新たなバイオマーカーの発見により、ゲノム医療はさらに発展し、より多くの乳がん患者に恩恵をもたらすことが期待されています。
このように、乳がん治療におけるゲノム医療は、個別化医療の重要な要素となり、今後も研究が進むにつれて、さらなる効果的な治療法が登場することが期待されます。
————————————————————

虎の門病院
虎の門病院乳腺内分泌外科の川端でございます。本日は乳がんのゲノム医療についてお話させていただきます。昨今『がんゲノム医療』という言葉は医療界のみならず、一般社会においても話題にされるようになりました。これは先進医療という枠組みで実施されてきた遺伝子パネル検査が昨年7月より保険償還され、いよいよ医療現場でルーティンに行われるようになったことを受けてのものです。昨年7月の日本乳癌学会総会、これは埼玉医科大学国際医療センター病院長の佐伯俊昭教授が主催された総会ですが、ここにおいてもがんゲノム医療がメインテーマに掲げられ、学会を挙げてこの新しい医療へのディスカッションが行われました。このようにがんゲノム医療はプレシジョンメディスン、すなわち精密医療や個別化医療の中心的役割を担うものとして期待されています。なお本日のテーマは乳がんのゲノム医療ということになっていますが、ゲノム医療はがん種横断的なアプローチであり、臓器にとらわれないことがそもそも重要な点であります。このため乳がんに特異的なゲノム医療があるわけではありませんので、がんゲノム医療について一般的なお話しをしたうえで、乳がんの事情について触れていきたいと思います。
<ゲノムという言葉>
まずゲノムという言葉ですが、この言葉は遺伝子をはじめとした遺伝情報の全体を表しています。Geneすなわち遺伝子と総体を表すラテン語の接尾語omeという言葉を組み合わせて作られた造語で、英語ではジノームと発音され、日本語表記ではゲノムとなります。
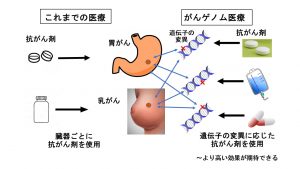
がんゲノム医療は、遺伝子情報に基づくがんの個別化治療のひとつです。がんゲノム医療は主にがんの組織を用いて多数の遺伝子を同時に調べていきます。これを「がん遺伝子パネル検査」といいますが、これにより遺伝子変異を明らかにし、一人一人のがんの性質などに合わせて治療を行うことががんゲノム医療です。
<遺伝子パネル検査>
一部のがんの治療では、すでに標準治療として、がんの組織などを用いて1つまたはいくつかの遺伝子を調べる「がん遺伝子検査」をコンパニオン診断として行い、遺伝子の変化に対応した薬、すなわち分子標的薬がこれまでも使われてきました。1つまたはいくつかの遺伝子を調べるがん遺伝子検査はがんゲノム医療ではありません。がんの組織を用いて一度に多数の遺伝子を調べるがん遺伝子パネル検査を行うことががんゲノム医療の重要な要素となっています。
【コンパニオン検査とがん遺伝子パネル検査の比較について】
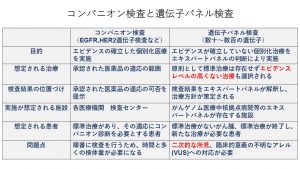
がん遺伝子パネル検査は、生検や手術などで採取されたがんの組織を用いて、次世代シークエンサーにより多数の遺伝子、通常は100~500遺伝子を同時に調べます。遺伝子変異が見つかり、その変異に対して効果が期待できる薬がある場合には、臨床試験などでその薬の使用を検討します。2019年7月からは2つのがん遺伝子パネル検査が保険償還されるようになりました。一つはOncoGuide™ NCCオンコパネルでがんに関連した114遺伝子を、がん組織と血液の両方で調べます。この場合は血液検査で遺伝性腫瘍に関連した遺伝子の異常が分かることがあります。もう一つはFoundationOne™ CDxがんゲノムプロファイルで、こちらはがんの組織の検査のみでがんに関連した324遺伝子を調べます。その他のがん遺伝子パネル検査も現在先進医療として行われており、新たに保険償還を目指して準備を進めています。がん遺伝子パネル検査の解析結果は複数の専門家から成るエキスパートパネルにより検討されその結果が担当医に報告されます。一般的に60%程度の患者さんに何らかの遺伝子異常を見出すことができ、具体的な治療薬に結び付く可能性は10-20%程度とされており、まだ開発途上のアプローチといえます。
<ゲノム医療の対象となる方>
がん遺伝子パネル検査は、がんの患者さんであれば誰でも受けられるわけではありません(2020年3月現在)。一般的には、①標準治療がない固形がん、②局所進行もしくは転移があり、標準治療が終了した、あるいは終了見込みの固形がんの人で、次の新たな薬物療法を希望する場合に検討します。また全身状態がある程度良好で、次の治療に耐えうるなどの条件もあります。このような制限を設けているのは限られた医療資源を有効に活用する目的と、乳がんのように確立された標準治療があるがん種で、早期に遺伝子パネル検査をして臨床的根拠の乏しい治療を行ってしまうことの弊害が懸念されているためです。これは今日新型コロナウイルスのPCR検査を希望者全例に行うことの是非の議論(2020年3月14日現在)と相通ずるものがあります。
<検査結果に基づく治療>
前述したようにがん遺伝子パネル検査を受けても必ず治療法が見つかるわけではありません。がん遺伝子パネル検査の前には、患者さんに十分次のようなことを理解していただく必要があります。即ち遺伝子変異が見つからない場合、あるいは見つかっても治療薬に結び付かないケースが前述のように多くあります。またがん遺伝子パネル検査では、多くの遺伝子を調べるため、本来目的とする個別化治療とは別に、がんになりやすい遺伝子をもっていることがわかる場合があり、これを二次的所見といいますが、医療側はこれに対して遺伝カウンセリングを行う体制を整える必要があります。検査に用いる検体については初回治療の手術などで摘出されたがんの組織を使用する場合が多いのですが、可能であれば現在の再発病巣などから新たに組織を採取した方が現在の病状の理解につながり有用と考えられています。
<がんゲノム医療が行われている206の病院>
がん遺伝子パネル検査は、がんゲノム医療の「中核拠点病院」、「拠点病院」、「連携病院」で行われています。2020年1月の時点で中核拠点病院は全国に11カ所、拠点病院は34カ所、連携病院は161か所あり、全国どこでもがんゲノム医療が受けられるようになることを目指して体制づくりが進められています。
<がんは遺伝子の病気である>
ここから改めていくつかの点を整理しておきたいと思います。がんは遺伝子に傷がついて起こる遺伝子の病気、すなわち遺伝子病ですが、決して子孫に遺伝はしない、すなわち遺伝病ではないという点です。がんは後天的に体細胞の遺伝子に傷がつくことによって起きる病気で、遺伝はしません。しかしながら生殖細胞系列の変異を介して、がんになり易いというリスクは遺伝します。例えば遺伝性乳がん卵巣がん症候群はこうした乳がんや卵巣がんになり易い遺伝子変異を先天的に持っている方たちのことを指しています。医師の方にはじっくり考えていただくと分かりやすい話ですが、一般の方には少し難しい話になるかもしれません。

The Okura Tokyo Aug. 2021
<がんゲノム医療というアプローチ>
人間の体の中で重量的にウエイトの大きい臓器は筋肉、脳、肝臓などですがこれらの細胞は細胞分裂をしません。粘膜、皮膚、血液などの一部の細胞だけが積極的に細胞分裂に関わっており、結果がんになる機会を招きます。ヒトの細胞はおよそ23000の遺伝子を持っており、これらの遺伝子はタンパク質を作る単位となっています。この23000の遺伝子の中でも増殖や、がん化に関わる遺伝子はごく一部で、逆にこの中にがんの弱点、アキレス腱があると考えられています。このアキレス腱を狙った治療薬が分子標的薬ですが、こうしたアキレス腱を効率よく見つけ、分子標的薬を効率よく使おうというアプローチががんゲノム医療ということになります。
<がんゲノム医療と国民皆保険>
日本におけるゲノム医療の特徴として、国民皆保険をベースにしていることが挙げられます。国民に等しく必要な医療を提供するという枠組みを維持することが重要で、アメリカのように患者が支払える保険に応じた医療を受けるというシステムとは根本が違っています。このことは重大な財政上の負担を意味し、少なくとも年間10万人規模の患者さんに適応できるシステムを構築する必要が生じます。一方で数年経てば、何十万人という規模のがん患者のゲノム情報、臨床情報が集まるという貴重な基盤を持つ国になるということも意味しており、このためにがんゲノム情報管理センター(C-CAT)を設立し情報を集める仕組みが作られて創薬などに生かされていく予定になっています。

<がんゲノム医療の実際の流れ>
臨床病院で患者さんの検体、臨床情報が集められ、検体は検査施設に送られ解析されます。その配列情報と臨床情報は前述のC-CATに集められ、ここで解析され臨床的意義づけのついたゲノム検査がん知識データベース報告書が中核拠点病院等のエキスパートパネルに送られ、そこで結果が解釈され、推奨する治療法などとともに各現場に情報が返されることになります。
<周術期乳がんの標準治療>
現在乳がんの病態に関連しては2つの主要な分子標的が明らかにされています。一つはエストロゲン受容体でこれはステロイドホルモン受容体であり転写因子です。エストロゲンによりエストロゲン受容体が活性化されると乳がん細胞内の腫瘍形成を促進させる経路が活性化されます。これと密接に関わるステロイドホルモンであるプロゲステロン受容体の発現もエストロゲン受容体のシグナル伝達活性化のマーカーです。ホルモン受容体が陽性と判断されれば、エストロゲン受容体シグナル伝達をダウンレギュレートするホルモン療法が第一選択の薬剤となります。
第二の分子標的はHER2(human epidermal growth factor 2)であり、これは細胞表面に存在する糖タンパクで受容体型チロシンキナーゼです。これは上皮成長因子受容体に類似した構造を持ちこの遺伝子が増幅又は過剰発現した乳がんはHER2陽性と分類され、抗体又は低分子阻害剤を用いた抗HER2療法の適応となっています。
こうして乳がんはホルモン受容体及びHER2の分子マーカーの有無により、3つの主なサブタイプに分類されており、ホルモン受容体陽性・HER2陰性群(約70%)、HER2陽性群(15%)、トリプルネガティブ即ち3つのマーカーがすべて陰性の群(約15%)の3群に分けられています。ホルモン受容体陽性の乳癌にはホルモン療法を行い、一部の患者さんには化学療法も行います。HER2陽性の患者さんはHER2をターゲットとした抗体や低分子阻害剤を用いた療法に化学療法を併用して行い、トリプルネガティブ乳がんの患者さんには化学療法のみを行うことが現在の治療体系となっています。
進行乳がんの治療
遠隔転移を伴う乳がんもサブタイプに応じて治療されますが、そのゴールは延命と症状の緩和になります。トリプルネガティブ乳がんの遠隔転移後の生存期間が2年程度であるのに対して、他の2つのサブタイプは平均5年程度とされており、適応となる薬剤の相違だけではなく、リスクプロファイルの明確な違いを前提とした対応が必要となります。現状の進行乳がんの治療は、病状とコンパニオン検査に基づく標準治療を一通り終えた患者さんに、がんゲノム医療という新しい可能性を見出す手段が加えられたということができます。

<乳がんのゲノム医療>
がんゲノム医療が進行乳がんの治療に導入されると、当然早い段階から遺伝子パネル検査を行い適切な治療法を検討したいという考え方が出てきます。実際アメリカではステージⅢ、Ⅳも遺伝子パネル検査の対象としています。しかしながら乳がんの早い治療ラインで遺伝子パネル検査を用いた治療選択を行うことに現在の標準治療を上回る効果があるという根拠は今のところなく、再発の早い段階での利用はすべて臨床試験の枠内で行うべきとされています。まずコンパニオン診断として10個以下のタンパク質、遺伝子を調べその結果と病状に適合した、即ち十分なエビデンスのある薬物療法を行い、治療法が限られてきた段階で遺伝子パネル検査を行って可能性のある薬物を探るというのが現在の標準的アプローチであるという認識を持っておくことが重要です。
<おわりに>
本日はがんゲノム医療の一般的なお話と、乳がん治療の中での位置づけのお話をさせていただきました。現状では実際に治療薬に結び付くケースは限られていますが、こうした医療が2019年に保険診療の枠内で開始されたというインパクトは大きく、近い将来患者さんたちへの福音となること、また日本独自の仕組みが創薬に大きく貢献できることを期待して本日のお話を終わりにしたいと思います。御清聴ありがとうございました。(2020年4月 日経ラジオの医学講座より)

