乳がんの化学療法(ケモセラピー)は、がん細胞の増殖や分裂を抑制・阻害するために抗がん剤を用いる治療法です。しかし、抗がん剤は正常な細胞にも影響を及ぼすため、多岐にわたる副作用が生じることがあります。これらの副作用は、患者の生活の質を低下させるだけでなく、治療の継続にも影響を与える可能性があります。本稿では、乳がん化学療法の主な副作用とその対処法について、詳細に説明します。
ホルモン療法
乳がんのホルモン療法について
1. はじめに
乳がんは、女性に最も多く見られるがんの一つであり、その治療には手術、化学療法、放射線療法、ホルモン療法などが含まれます。乳がんには、エストロゲンやプロゲステロンといったホルモンによって成長が促されるタイプがあり、このようなホルモン依存性の乳がんに対して、ホルモン療法(内分泌療法)が有効です。本稿では、乳がんのホルモン療法の概要、そのメカニズム、種類、適応、副作用、そして治療後のフォローアップについて詳しく説明します。
2. ホルモン療法とは
ホルモン療法は、がん細胞の増殖を促進するホルモンの作用を抑制し、がんの進行を防ぐ治療法です。特に乳がんでは、エストロゲンやプロゲステロンという女性ホルモンが、がん細胞の成長に大きな役割を果たす場合があります。このホルモン依存性乳がんに対して、ホルモン療法は効果的です。ホルモン療法の目的は、体内のホルモンの生成やその働きを抑えることで、がん細胞の成長を阻止することです。
乳がんのホルモン療法は、がんがホルモン受容体陽性(エストロゲン受容体陽性またはプロゲステロン受容体陽性)である場合に効果的であり、治療計画の中で重要な役割を果たします。ホルモン受容体陽性の乳がんは、全乳がんの約70%を占め、特に閉経後の女性に多く見られます。
3. ホルモン療法のメカニズム
ホルモン療法は、主にエストロゲンの作用を抑えることでがん細胞の増殖を防ぎます。乳がん細胞の多くは、エストロゲンやプロゲステロンといったホルモンを「栄養源」として成長するため、これらのホルモンの受容体を持っています。エストロゲン受容体やプロゲステロン受容体ががん細胞の表面に存在すると、体内で分泌されるホルモンがこれらの受容体に結合し、がん細胞が増殖します。
ホルモン療法は、以下の3つの主要なメカニズムを通じてエストロゲンの働きを阻害します。
- エストロゲンの生成抑制: エストロゲンの生成そのものを抑制することで、がん細胞へのエストロゲン供給を減少させます。主に閉経後の女性に対して、アロマターゼ阻害剤が用いられます。
- エストロゲン受容体のブロック: 乳がん細胞のエストロゲン受容体に結合して、エストロゲンが受容体に結びつくのを阻止します。これにより、がん細胞の成長が抑えられます。タモキシフェンなどの選択的エストロゲン受容体調節薬(SERM)がこの役割を果たします。
- エストロゲンの分泌を阻害: ホルモンの生成や分泌を調整する視床下部や下垂体に作用して、エストロゲンの分泌を抑える薬剤もあります。リュープロレリンなどのゴナドトロピン放出ホルモン(GnRH)アゴニストがこれに該当します。
4. ホルモン療法の種類
ホルモン療法にはいくつかのアプローチがあります。患者の年齢、閉経状態、がんのステージやホルモン受容体の状況などによって、適切な治療が選択されます。主なホルモン療法の種類を以下に示します。
4.1 タモキシフェン(選択的エストロゲン受容体調節薬: SERM)
タモキシフェンは、エストロゲン受容体をブロックすることによって、がん細胞にエストロゲンが作用するのを防ぎます。この薬剤は閉経前および閉経後の女性の両方に対して使用され、特にホルモン受容体陽性の早期乳がんや進行乳がんに対して効果があります。
タモキシフェンは、特定の組織ではエストロゲンの作用を抑える一方で、他の組織ではエストロゲンの作用を模倣する特徴があります。たとえば、骨や子宮ではエストロゲンのように働き、骨密度を保つ一方で、乳腺組織ではエストロゲンの効果を抑えるという独特な作用を持っています。
4.2 アロマターゼ阻害剤
アロマターゼ阻害剤は、主に閉経後の女性に使用される薬剤です。アロマターゼという酵素を抑制することで、体内でアンドロゲンからエストロゲンに変換される過程を阻害し、エストロゲンの生成を減少させます。このタイプの薬には、レトロゾール、アナストロゾール、エキセメスタンなどがあります。
閉経前の女性では卵巣が依然としてエストロゲンを分泌しているため、アロマターゼ阻害剤は効果的ではありませんが、閉経後の女性では体脂肪組織などでアロマターゼがエストロゲンを生成しており、これががんの成長を促進するため、アロマターゼ阻害剤は有効です。
4.3 ゴナドトロピン放出ホルモン(GnRH)アゴニスト
GnRHアゴニストは、視床下部からのホルモン分泌を調整し、間接的に卵巣からのエストロゲンの分泌を抑制します。この治療法は、閉経前の女性においてエストロゲンレベルを低下させるために使用されます。代表的な薬剤には、リュープロレリンやゴセレリンがあります。これにより、一時的に閉経状態を誘導し、エストロゲン依存性の乳がんの成長を抑える効果があります。
4.4 フルベストラント(エストロゲン受容体拮抗薬)
フルベストラントは、エストロゲン受容体を完全に破壊することで、エストロゲンの作用を抑える薬剤です。通常は、タモキシフェンやアロマターゼ阻害剤の効果が不十分な場合に使用されます。フルベストラントは、特に閉経後の女性の進行性乳がんに対して使用されます。
5. 適応
ホルモン療法は、乳がんの治療において以下のような状況で適応されます。
- 早期乳がん: 手術や放射線療法後の補助療法として使用され、再発のリスクを低減します。
- 進行乳がん: がんが進行している場合でも、ホルモン療法によってがん細胞の増殖を抑制することが期待されます。
- 予防: 乳がんの家族歴がある高リスク女性に対して、予防的にホルモン療法が行われることもあります。たとえば、タモキシフェンは高リスクの閉経前後の女性に対して予防的に使用されることがあります。
6. 副作用
ホルモン療法は、乳がんの治療において有効ですが、患者によっては副作用が発生することがあります。副作用の種類や程度は、使用する薬剤や患者の体質によって異なります。
6.1 タモキシフェンの副作用
タモキシフェンの主な副作用は以下の通りです。
- 更年期症状: ほてり、発汗、月経不順など、更年期に似た症状が出現することがあります。
- 血栓症: 深部静脈血栓症や肺塞栓などのリスクがわずかに増加します。
- 子宮内膜癌: タモキシフェンは子宮内膜にエストロゲン様作用を持つため、子宮内膜癌のリスクがわずかに増加する可能性があります。
6.2 アロマターゼ阻害剤の副作用
アロマターゼ阻害剤の副作用には以下のものがあります。
- 骨密度の低下: エストロゲンが骨密度を保つ役割を果たしているため、アロマターゼ阻害剤によるエストロゲンの減少が骨粗鬆症や骨折のリスクを高めます。
- 関節痛や筋肉痛: 関節や筋肉の痛みが出ることがあります。
- 脂質代謝の異常: コレステロール値の上昇など、脂質代謝に影響を及ぼすことがあります。
6.3 GnRHアゴニストの副作用
GnRHアゴニストの使用により、一時的に閉経状態が誘導されるため、以下のような副作用が出ることがあります。
- 更年期症状: ほてり、発汗、骨密度の低下、気分の変動など。
- 性欲の低下: エストロゲンの低下に伴い、性欲が減少することがあります。
7. 治療後のフォローアップ
ホルモン療法を受けた後も、定期的なフォローアップが重要です。特に、副作用の管理や治療効果のモニタリングが必要となります。
7.1 定期的な検査
ホルモン療法の効果を評価するために、定期的な画像検査や血液検査が行われます。また、骨密度の検査も、骨粗鬆症のリスクを評価するために定期的に実施されることがあります。
7.2 副作用の管理
治療中に発生する副作用は、適切な管理が必要です。たとえば、骨密度が低下した場合、カルシウムやビタミンDの補給、さらには骨を強化する薬剤の使用が検討されます。
7.3 ライフスタイルの調整
ホルモン療法を受ける患者は、健康的なライフスタイルを維持することが推奨されます。特に、バランスの取れた食事や適度な運動が、骨密度の低下を予防するのに役立ちます。
8. 結論
乳がんのホルモン療法は、ホルモン受容体陽性の乳がん患者に対して非常に有効な治療法です。エストロゲンの作用を抑えることで、がんの進行や再発を防ぎます。治療の選択は、患者の年齢や閉経状態、がんのステージによって異なりますが、タモキシフェン、アロマターゼ阻害剤、GnRHアゴニストなどの薬剤が主に使用されます。一方で、治療には副作用も伴うため、定期的なフォローアップと副作用の管理が重要です。乳がん患者にとって、ホルモン療法は長期にわたる治療になることが多いため、患者が治療に対して理解を深め、医療チームと連携して治療を継続することが大切です。
以上、2024年10月作成
——————————————

虎の門病院
ホルモン療法はなぜ効くか
女性ホルモンの働きを阻害
乳がんの7割は、ホルモン依存性で、エストロゲンという女性ホルモンの影響で増殖します。
そこで、体内のエストロゲンの量を減らしたり、エストロゲンの働きを阻害して、がんの増殖を止めて萎縮させてしまうのが、ホルモン療法です。
実際には、ホルモン依存性の乳がんには、「ホルモン受容体」という目印があります。女性ホルモンとホルモン受容体は、鍵と鍵穴のような関係にあり、女性ホルモンはこの受容体に結合することで、細胞にさまざまな命令を下し、ホルモンとしての作用を発揮します。
そこで、手術後に摘出したがんの組織を検査して、ホルモン受容体の有無を見ます。ホルモン受容体には、エストロゲン受容体とプロゲステロン受容体という2種類があります。この両者がある場合、あるいはどちらか一方でもある場合には、積極的にホルモン療法が行われます(実際にはエストロゲン受容体が陰性で、プロゲステロン受容体が陽性ということはまれとされています)。これを、エストロゲン受容体陽性、あるいはエストロゲン感受性あり、といったいい方をします。
逆に、どちらのホルモン受容体もなければ、エストロゲン受容体陰性、エストロゲン感受性なし、といいます。受容体がなければ、そのがんは女性ホルモンの影響とは関係なく増大するがんなので、ホルモン療法は効かないと考えます。
ホルモン剤は、抗がん剤のような強い副作用がないのが大きな利点ですが、受容体がない人に投与しても、副作用はあってもがんに対する効果はほとんどないのです。
ホルモン感受性がある人に、術後補助療法としてホルモン療法を行うと、転移や再発がほぼ半分に減ることがわかっています。
ホルモン剤には4種類ある
ホルモン剤には、体内のエストロゲンの量を減らす薬と、エストロゲンの働きを阻止するものがあります。さらに、閉経前と閉経後ではホルモン環境が大きく異なるので、これに合わせてホルモン剤を選択します。
抗エストロゲン薬
エストロゲンの働きを阻止する薬です。
エストロゲンは、細胞表面にあるエストロゲン受容体に結合することで、細胞にさまざまな命令を下しています。この受容体に結合して、エストロゲンが結合するのをブロックするのが、抗エストロゲン薬です。それによって、エストロゲンの作用が阻止され、がんの増殖を抑えます。
術後補助療法に使われる代表的なホルモン剤に「タモキシフェン」がありますが、これも抗エストロゲン薬の一つです。タモキシフェンは、20世紀の乳がん治療における最大の発見の一つともいわれ、Ⅰ~Ⅱ期の乳がんでは、術後補助療法にタモキシフエンを使うと、生存率が絶対値で6~10%向上するというデータが出ています。
タモキシフェンは、乳がんの再発率を下げるだけではなく、反対側の乳房にがんが発生する率を2.4%から1.6%に減らす、コレステロールを低下させ心血管系の障害を予防する、骨粗鬆症@こつそしようしよう@を予防する、といった作用もあります。閉経前、閉経後どちらにも効果があります。内服薬で、毎日1回、通常5年間服用します。
ほかに同系統の薬として「トレミフェン」というホルモン剤もあり、こちらは閉経後に使われます。
LH-RHアゴニスト
閉経前の女性に投与して、エストロゲンの量を減らすホルモン剤です。
エストロゲンは卵巣でつくられますが、それまでに脳から次々に指令が送られています。まず、脳の視床下部@ししようかぶ@という部位から性腺刺激ホルモン放出ホルモン(LH-RH)が分泌されて、下垂体@かすいたい@を刺激します。その刺激で、下垂体からは性腺刺激ホルモンが分泌されて卵巣を刺激。その結果、卵巣からエストロゲンが分泌されるのです。
LH-RHアゴニストは、この最初の段階で作用する薬です。性腺刺激ホルモン放出ホルモンも、下垂体の受容体に結合して、性腺刺激ホルモンを分泌させます。LH-RHアゴニストは、性腺刺激ホルモン放出ホルモンが下垂体の受容体に結合するのを邪魔して、下垂体から卵巣にエストロゲンの分泌命令が出されるのを阻止するのです。
タモキシフェンと併用することもよくあります。通常は2年~5年間使います。その間は生理が止まりますが、投与をやめると、卵巣機能が回復して生理が戻るのも特徴です。この薬は注射薬で、月に1度打つタイプと、3カ月に1度打つタイプがあります。
ゴセレリンやリュープロレリンというホルモン剤がこのタイプです。
アロマターゼ阻害薬
エストロゲンの量を減らすホルモン剤で、閉経後の女性に効果があります。
閉経後は、卵巣でのエストロゲンの分泌は停止しますが、副腎でつくられるアンドロゲンという男性ホルモンが、脂肪細胞などでエストロゲンにつくり変えられます。このとき働くのが、アロマターゼという酵素@こうそ@です。そこで、アロマターゼの働きを阻害して、男性ホルモンからエストロゲンがつくられないようにするのが、アロマターゼ阻害薬です。
アロマターゼ阻害薬には、アナストロゾール、エキセメスタン、レトロゾールなどがあります。
プロゲステロン製剤(黄体ホルモン製剤)
間接的にエストロゲンの量を減らしますが、その作用はよくわかっていない部分も多く、ほかのホルモン剤が効かないときに使われます。
(タモキシフェンの再発率低下などのデータ、ホルモン剤の一覧表)
閉経とホルモン療法の進め方
抗がん剤と効果は同等
術後に行われるホルモン療法には、現在3種類のホルモン剤が用いられますが、閉経前か閉経後かによって、選ばれる薬は異なります。閉経とは、60歳以上であるか、45歳以上で過去1年以上生理がない場合、または両側の卵巣を2個とも摘出している場合、と定義されています。子宮摘出を受けている場合は血中のホルモン値を参考にして決めます。E2(エストラジオール)が低値で、FSH(卵胞刺激ホルモン)が高値の場合は閉経と考えます。
タモキシフェンは、閉経前か閉経後かにかかわらず使われますが、LH?RHアゴニストは閉経前、アロマターゼ阻害薬は閉経後に使われるホルモン剤です。
閉経前
LH?RHアゴニストは、1カ月に1回か3カ月に1回、皮下注射で投与します。2~5年間継続するのが一般的です。CMF(シクロホスファミド、メトトレキサート、5-FUの3剤を併用)という組み合わせの抗がん剤を6カ月投与した場合と、2年間LH?RHアゴニストを注射した場合で効果を比較すると、再発を抑える効果は同等です。タモキシフェンと併用すると、AC(アドリアマイシンとシクロフォスファミドの2剤を併用)やCAF(シクロホスファミド、アドリアマイシン、5-FUの3剤を併用)という抗がん剤治療と同等の再発抑制効果があります。抗がん剤よりは副作用が少なく、同じ程度の効果が得られるのが大きな利点です。
より効果が高いホルモン剤へ
閉経後乳がんの術後補助療法は、タモキシフェンがかつては標準治療でしたが、アロマターゼ阻害薬の方が効果が高いことがわかり、こちらが標準治療となっています。
閉経後
アロマターゼ阻害薬には、現在3種類ありますが、どれも効果は同じ程度です。
以前は、閉経後もタモキシフェンによる再発予防効果が最も高いとされていました。ところが、タモキシフェンを5年間服用するより、アロマターゼ阻害薬(アナストロゾール)を5年間服用したほうが再発率が13%低く、副作用も少ないことが報告され、大きな反響を呼びました。
またその後、タモキシフェンを2~3年服用したあとでアロマターゼ阻害薬(エキセメスタン)に切りかえて、計5年間治療をつづけると、5年間タモキシフェンをつづけるより再発率が32%も低下すること、さらにタモキシフェンを5年間服用したあとでアロマターゼ阻害薬(レトロゾール)を5年間つづけると、再発率がさらに40%も低くなるなど、次々にアロマターゼ阻害薬の効果が報告されています。
蓄積されたデータから、現在は閉経後乳がんの術後補助療法にアロマターゼ阻害薬を最初から使うことが標準となっています。
ホルモン剤の副作用
半数に更年期障害が
ホルモン療法は、抗がん剤にくらべて副作用が少なく、それでいて高い効果があるのが大きなメリットです。とはいえ、ホルモン療法にもまったく副作用がないわけではありません。
更年期障害
ホルモン療法は、簡単にいえば、エストロゲンの量を下げる治療法です。その結果、ちょうど閉経と似た状態になり、更年期障害のような症状を訴える人が少なくありません。
ホットフラッシュが起きて冬でも汗が吹き出たり、動悸@どうき@や不安、睡眠障害、イライラ、抑うつ症状などを訴える人もいます。ホットフラッシュは、軽いものも含めると、ホルモン療法を行った人の半数以上にあらわれます。
しかし、ここで更年期障害の治療のためにホルモン補充療法をしたのでは、ホルモン療法の意味がなくなってしまいます。ほんとうの更年期と同じで、少しがまんしていれば、体がエストロゲンの低い状態に慣れて楽になってくるはずです。がまんできないほどつらければ、更年期障害に使われる漢方薬を使ったり、うつ状態には抗うつ薬を使うこともあります。
また、アロマターゼ阻害薬はタモキシフェンよりホットフラッシュが出る率が低いので、閉経と判断できれば早めにアロマターゼ阻害薬にかえるのも一つの方法です。
生殖器の症状と子宮体がん
タモキシフェンには、子宮内膜の増殖作用があるため、不正出血が起こることがあります。それ自体はあまり心配ありませんが、タモキシフェンは、子宮体がんのリスクを高めることがわかっています。といっても、800人に1人の割合だった発生率が800人に2~3人に増えるという程度です。その鑑別のために、不正出血がつづくようならば、検査を受けましょう。
一方で、タモキシフェンは、10年間で乳がんの再発を相対的に45%抑えることができます。再発予防効果が副作用のデメリットを超えるからこそ、タモキシフェンが使われるのです。子宮体がんは、不正出血により早期発見が可能です。またタモキシフェンに誘発される子宮体がんは比較的悪性度が低く、早期に見つかれば手術で治る可能性が高いとされています。しかし、乳がんは再発してしまえば、完治は困難です。
骨粗鬆症
アロマターゼ阻害薬やLH?RHアゴニスト製剤は、エストロゲンの量を減らすため、更年期以降と同じように骨量が減少し、骨粗鬆症になりやすくなることがわかっています。反対に、タモキシフェンは骨量を増やして骨をじょうぶにする作用があります。
骨量が低下してきた場合には、骨量を増やす薬を併用します。
アロマターゼ阻害薬で、関節の痛みやこわばりが出ることがありますが、これも時間経過で軽快する場合が多いようです。
その他
このほか、タモキシフェンではまれに下肢@かし@に血栓(血の固まり)ができたり、それが肺に詰まって肺動脈塞栓症を起こすことがあるため、静脈血栓症の既往@きおう@がある人へのタモキシフェンの使用は特に注意が必要です。
月別アーカイブ:
年別アーカイブ:
化学療法(抗がん剤治療)
抗がん剤の作用とは
ホルモン剤が、エストロゲンという、いわばがんの増殖に必要な栄養源を断ち切って再発や転移を防ぐのに対し、抗がん剤はその毒性でがん細胞を殺傷する薬です。
抗がん剤は、がん細胞の遺伝子や細胞増殖機能などを障害して、死に至らしめます。手術や放射線治療などの局所治療を行うと、残ったがん細胞に増殖の刺激をあたえる可能性が考えられています。この刺激によって、全身に散ったがんの芽、つまり微小転移したがん細胞が活性化し、増殖すると考えられているのです。
しかし、細胞が分裂・増殖するためには、さまざまなシステムが機能し、外からもいろいろな材料を補充する必要があります。細胞としては不安定なこの時期に、毒性を持った抗がん剤を投与して、がんの芽をつぶしてしまおうというのが、抗がん剤による術後補助療法の考え方です。
一方で、抗がん剤の毒性は正常細胞にも同じように作用します。そのために、抗がん剤によるさまざまな副作用が起こります。特に、がんと同じように分裂スピードの早い毛髪をつくる細胞や骨髄細胞、粘膜細胞、生殖細胞などはダメージを受けやすいことがわかっています。脱毛や吐き気、嘔吐、下痢、白血球数の減少など、抗がん剤に多い副作用はこうして起こるのです。
それでも、正常細胞はがん細胞より毒性に対する抵抗力があり、回復力も強いので、治療では正常細胞が耐えられる範囲内で、がん細胞が死ぬ量の抗がん剤が投与されます。
抗がん剤は組み合わせて使う
抗がん剤を使う場合に重要なのが、その組み合わせです。
抗がん剤には毒性があるので、一種類の抗がん剤を多量に使うと、特定の副作用だけが強く出てしまう危険があります。そこで、効果のある抗がん剤を数種類(ふつうは2~3種類)組み合わせて使うのが、多剤併用療法の考え方です。薬を組み合わせることで副作用の危険を減らし、複合的な効果が高まると考えられています。
どの抗がん剤の組み合わせや使用法が一番効果的なのか、そしてその副作用は許容できるものなのか、患者さんの協力を得て大規模な臨床試験が行われています。その結果、現在の時点で一番効果的な薬の組み合わせと投与法が「標準治療」となります。
こうした抗がん剤の組み合わせは、抗がん剤の英語の頭文字をとって、AC(Aはアドリアマイシン、Cはシクロフォスファミド)とか、TC、CEFといった呼び方をされます。「(○ページ参照)。
乳がんの領域ではアドリアマイシン系の抗がん剤と、タキサン系の抗がん剤が骨格となっていくつかの標準的な治療法が確立されています。
抗がん剤治療の進め方
《休薬期間をおいて治療》
抗がん剤は複数の薬を組み合わせて使いますが、もう一つ大切なポイントは、休薬期間をおいて治療をくり返すということです。
1週間に1回、あるいは3週間に1回投与し、その間は休んでこのサイクルを何回かくり返します。
抗がん剤すると、がん細胞も障害されますが、正常細胞もダメージを受けます。ここで休薬期間をおくと、正常細胞は回復して元気になりますが、がん細胞は回復能力が欠けているため、十分回復しません。そこで、1~3週間休んで正常細胞が元気になったころに、また抗がん剤治療をくり返してがん細胞をたたくわけです。
抗がん剤の種類によって、投与のしかたは様々ですが、1回の治療を1クールとか1サイクルというふうにいいます。6サイクルといえば、休薬期間をおきながら6回抗がん剤治療をくり返すという意味です。
《術後治療でよく使われる抗がん剤》
では、抗がん剤にはどのような種類があり、どのような使われ方をするのでしょうか。
抗がん剤には、点滴などで体内に入れる注射薬と飲み薬があります。乳がんの術後補助療法では、ACやTCという組み合わせによる併用法、あるいはAC4サイクルに引き続き、タキサン系の4サイクル(AC→T療法)というような連続投与法が、よく行われています(表参照)。
JNCCN2011年3月号より
アメリカでHer2陰性の患者さんに用いられている抗がん剤治療法の頻度を図にしたものです。TC療法とAC→T療法が治療法を2分しており、その他をTAC療法、AC療法、CMFが占めています。
アンスラサイクリン系
乳がん治療に古くから使われている抗がん剤で、直接遺伝子を破壊してがん細胞を殺傷します。アドリアマイシン、エピルビシンなどの薬があり、アドリアマイシンを含む併用療法には、ACやFAC、エピルビシンを含む併用療法には、EC、FECといった治療法があります。
タキサン系
細胞の分裂過程を阻害する薬で、パクリタキセルとドセタキセルがあります。これらの薬は単独で使ったり、ほかの薬と併用して用います。
アルキル化薬
遺伝子に作用する薬で、シクロフォスファミドはアンスラサイクリン系の薬などと組み合わせて使われます。
その他
細胞の分裂過程を阻害するビノレルビン、遺伝子合成を抑える5?FU(フルオロウラシル)やメトトレキサートなどがあります。
《期待される再発抑制効果》
抗がん剤を投与すると少なくとも多くの患者さんに一時的な効果を認めるため、なるべく多くの患者さんに行われた時期もありました。しかし現在では抗がん剤を行うことによる生存率の改善効果は限られた患者さんに大きく、一方あまり効果がない患者さんも分かってきたため、副作用とのバランスを考え、効果が期待できる患者さんに対象が絞られるようになってきました。
やや専門的な話で恐縮ですが、抗がん剤の効果は次のようにして考えられています。①抗がん剤が効くタイプかどうか? これにより相対的な再発抑制効果(relative risk reduction)を推計します。②抗がん剤を行わなかった場合、どの程度の再発が予測されるか?これをベースラインリスク(baseline risk)と呼びます。①と②を掛け合わせたものが、実質的な再発抑制効果(absolute risk reduction)となります。再発の可能性が40%ある患者さんに、再発抑制効果が30%ある治療を行うと0.4×0.3=0.12となり12%の人が救われるという推計を行います。この数字が大きいほど、副作用を覚悟で、抗がん剤を行った方がよいということになりますし、この数字が小さければ、治療の意味があまりないということになります。
再発抑制効果が高いということは良い治療といえるし、たとえ再発抑制効果が大きくても、あまり再発しない患者さんに治療しても、成果が上がらないことがおわかりいただけると思います。
乳がんのタイプ別の治療法
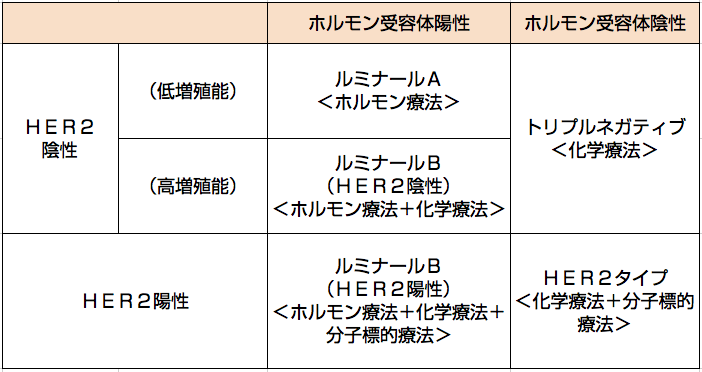
コラム 大切な初期治療
がんが発見されて最初に行う治療を「初期治療」といいます。再発や転移によって、2回、3回と治療を繰り返す場合の治療と区別するためにこのような言い方をします。
抗がん剤治療でも、初回の治療が大切です。薬物治療がうまくいかず、臓器転移をおこした場合は、その後の治療によって、一時的な症状の改善はみられても、治癒の可能性が極めて少なくなるからです。
全身に転移したがんの量(腫瘍量)が少ない場合は、薬物療法による完治の期待がありますが、レントゲンなどで診断できるほどの臓器転移が成立した場合は、完治は困難になります。したがって乳がんの薬物療法は先手必勝、緒戦の勝利が絶対条件になるのです。
ただ抗がん剤はそれなりの副作用があるため、そもそも効かない人には必要ないし、抗がん剤をやらなくても再発しない人にも必要ないということが言えます。抗がん剤の効果が期待でき、なおかつ再発のリスクがある人には、最適なスケジュールと量で妥協なくやり切るというメリハリが重要なのです。
月別アーカイブ:
年別アーカイブ:
乳がん化学療法の副作用と対処法について
—————————————–

虎の門病院
脱毛や吐き気、白血球減少
抗がん剤には、個人差はありますが、それぞれに副作用があります。しかし、ある程度副作用の傾向も決まっているので、現在はその対処のしかた、予防の方法もずいぶん進歩しています。このためあまりこわがらないでもだいじょうぶです。まず、主な薬剤の代表的な副作用を見てみましょう。
AC療法(同系統のものにEC療法、FAC療法、FEC療法があります)
3週ごとに通常4回の点滴(4サイクル)を行います。
1990年代以降、標準的な投与法として幅広く用いられてきました。現在はTC療法に置き換わりつつあります。アドリアマシン(A)を類似薬のエピルビシン(E)に代えたのがEC療法で、さらに5-FUを組み合わせたのがFAC療法、FEC療法です。3週間に一度の点滴を計4回行います。短期間で終わることが利点ですが、脱毛と吐き気が副作用として問題になります。
TC療法
AC療法のアドリアマイシンをタキソテールに置き換えたのがTC療法で、2006年末の論文発表から使用頻度が増えてきました。元々アメリカで研究が進んだ経緯があり、4サイクルの抗がん剤としてはアメリカではTC療法が主流ですが、ヨーロッパではまだまだEC療法、FEC療法が健闘しており、日本がその中間くらいの状況です。主な副作用としては脱毛、全身倦怠感、皮疹、末梢神経障害などが知られています。
AC→T療法(同系統のものにFEC→T療法)
AC療法やFEC療法を4サイクル行った後、引き続きタキソテールやタキソールを投与する方法です。再発のリスクが高く、化学療法の効果が高いと予想される患者さんに用いられます。副作用の内容としてはAC療法、TC療法と大きくは変わりませんが、治療が長期に及ぶ分、副作用もきつくなります。
以上の3タイプの他にはTAC療法やCMF療法が行われています。TAC療法はアメリカで主に行われており、CMF療法は1980年代~90年代に行われた治療法で、効果はやや落ちますが副作用の少なさが評価され今でも高齢者に行われる場合があります。
主な副作用とその対策
副作用は、抗がん剤の効果と比例するものではなく、副作用が強いから効果も高いというわけではありません。ですから、副作用はがまんしないで、薬で抑えたり、適切な対策をとって乗り切りましょう。
吐き気・嘔吐
吐き気も個人差が大きいのですが、アドリアマイシンやエピルビシン、シクロフォスファミドなど、吐き気が出るリスクが高い抗がん剤を使う場合には、抗がん剤の点滴をする前に、吐き気止めを注射や内服で用います。
5-HT3受容体拮抗剤、副腎皮質ステロイドホルモンが主に用いられていますが、最近では新規5-HT3受容体拮抗剤のパノロセトロン、NK1受容体拮抗剤のアプレピタントが使用可能になり、抗がん剤のタイプによって選択の幅が広がりました。
また、一度強い吐き気を経験すると、化学療法が始まると思っただけで吐き気が出てしまう(予期性嘔吐)ことがあります。この予防にはもちろん嫌な経験を一度でもしないようにすることが重要ですが、抗不安薬などの内服により緩和できることが知られています。
【日常生活でできる工夫】
☆抗がん剤を投与する日の食事は、軽めにする。
☆食事を少しづつとり、一度に満腹にならないようにする。
☆ 食事や飲み物は、ゆっくりとる。
☆油っぽいものや消化の悪いものは避ける。
☆臭いによるムカツキを防ぐには、食べ物を冷やしたり、冷ましてから食べるとよい。
☆リンゴジュースやグレープスルーツジュースを冷やして飲んだり、氷を口に含む。
☆食後はすぐに横になるより、1時間ぐらい椅子に座って休む。
☆映画を見たり、音楽を聞く、おしゃべりをするなど、好きなことに集中して気分転換をはかる。
白血球の減少や貧血など骨髄抑制
抗がん剤によって、血液中の血球成分をつくる骨髄の働きが低下するために起こる副作用です。白血球が減少すると、免疫@めんえき@が低下して病原菌に感染しやすくなります。そのために、カゼや肺炎、発熱、虫歯の痛みやはれ、食中毒などにもかかりやすくなります。
ふつう、白血球は抗がん剤を投与して1週間前後から低下しますが、3週間ほどで回復します。実際に感染を起こすことは少なく、発熱など感染があった場合には、抗生剤で治療します。白血球(好中球)の量が減少しすぎた場合には、白血球を増やす薬を使ったり、抗がん剤の量を減らしたり、しばらく治療を休んだりして対処します。
赤血球が減少すると、貧血になってだるくなったり、息切れを感じることもあります。血小板が減少すると、出血しやすくなるので、鼻血や歯茎からの出血、下血などがあったら、医師や看護師に相談してください。
【日常生活でできる工夫】
☆治療中は、人が多い場所にはなるべく行かない。
☆外出したら、手洗いとうがいを忘れずに。
☆38度以上の発熱があったら、医師、看護師に相談する。
☆膀胱炎やカゼ症状など、感染症状に気づいたら病院へ。
脱毛
外見が変わってしまうので、精神的にも非常にストレスが大きいのが脱毛です。髪の毛だけではなく、眉毛や体毛まで抜けてしまうこともあります。
残念ながら、脱毛を根本から防ぐ手段はありません。ただ、ちょっとした工夫で、気持ちをやわらげることはできます。そして、治療が終わればすぐに毛がはえてきて、元通りになることを忘れないでください。
【日常生活でできる工夫】
☆朝起きたとき、寝具にたくさん毛髪が落ちていたり、シャンプーやブラッシングのときに大量に毛が抜けるのは、決して気持ちのよいものではありません。できれば、治療前に髪を短くしておきましょう。
☆シャンプーは刺激の少ないものに。
☆ブラシはやわらかいものに。
☆パーマや毛染めはお休みに。
☆あらかじめ、気に入った帽子やバンダナを用意して。
☆脱毛が起きる前に、カツラを用意する。
口内炎や味覚の変化
抗がん剤による口内炎は、口の中がただれたり、潰瘍@かいよう@ができて、痛みで食事をとれないほどひどくなることもあります。そのために、病原菌の感染が起こることもあります。こうしたときは、局所麻酔薬の入ったうがい薬を使ったり、鎮痛剤を使います。
【日常生活でできる工夫】
☆やわらかい食事や流動食にする
☆口の中を清潔にしておく。うがいは、起床時、毎食後、就寝前など、1日7~8回以上を目安に。
☆歯磨きはやわらかい歯ブラシを使う。
☆可能ならば、化学療法をはじめる前に歯科医で歯の掃除を。
また、苦みを感じたり金属のような味がしたり、味覚の低下や過敏になるなど、味覚にも異常が起こることがあります。味覚異常には亜鉛@あえん@が効くことがあるので、医師や看護師に相談してみましょう。
フルオロウラシルやカペシタビンなどの抗がん剤は、「手足症候群」を起こすことがあります。手足の裏が刺すように痛んだり、感覚が鈍る、発赤@ほつせき@や発疹@ほつしん@、かゆみなどが出て患者さんを悩ませます。保湿クリームやステロイドの塗り薬で軽減することもありますが、ひどい場合は薬の量を減らしたり、中止することもあります。
その他
このほか、下痢やむくみ、便秘、関節や筋肉の痛み、タキサン系の抗がん剤では、手足のしびれやピリピリ感、刺すような痛み、感覚が鈍くなるなど、末梢神経傷害があらわれることがあります。まだこれを防ぐ薬はありませんが、治療が終われば多くは改善していきます。
☆ コラム 副作用からの回復
抗がん剤には、さまざまな副作用があり、健康なときならばあまり深刻には考えない口内炎やしびれ、皮膚の発疹なども、ひどくなると治療を中断しなければならないこともあります。
ただし、治療が終わればほとんどの症状は回復していきます。そのスピードは、副作用の種類によっても異なりますが、たとえば皮膚の症状や毛髪などは、細胞の入れかわる速度が速いので、治療を終えて数週間で回復してきます。とはいえ、髪の毛を伸ばすのと同じですから、元の髪形に戻るには何カ月かかかります。
タキサンによるしびれや手足の感覚異常などは、もう少し時間がかかって、治療終了後9カ月以内に半数の人が回復すると報告されています。
月別アーカイブ:
年別アーカイブ:
分子標的治療薬とは
がん細胞をねらい撃ち
抗がん剤が、その毒性でがん細胞も正常細胞も無差別に攻撃するのに対し、がん細胞の生物学的特性に的@まと@をしぼって攻撃するのが、「分子標的治療薬」です。
分子レベルでがんの研究が進んだ結果、がん細胞ががん細胞であるためには、いろいろなメカニズムが必要であることがわかってきました。栄養を取り込むために、にわかづくりの血管を引き込んだり、どんどん分裂増殖したりします。こうしたメカニズムに的をしぼって、がん細胞をねらい撃ちするのが、分子標的治療薬です。正常細胞には、こうした特性はないので、攻撃目標にはなりません。
そのため、分子標的治療薬には、これまでの抗がん剤のような副作用はあまり認めません。ただし、別の副作用が出ることはあります。
分子標的治療薬は、がんの薬物療法に新たな選択肢を設け、治療法を大きく前進させました。現在、がんのメカニズムが解明されるとともに、さまざまな分子標的治療薬が開発され、治療に使われています。なかでも最も成功した分子標的治療薬の一つが乳がんに使われる「トラスツズマブ」(商品名ハーセプチン)です。
以前は悪性といわれたタイプ
トラスツズマブは、がん細胞の表面にあるHER2という受容体(HER2タンパク)に結合して、増殖を阻止する抗体治療薬です。
エストロゲンが、細胞表面にあるホルモン受容体に結合してホルモンとして作用するように、HER2受容体に作用物質が結合すると、細胞に増殖命令が出ます。正常細胞にもHER2受容体はあるのですが、乳がん細胞の中にはHER2受容体が異常にたくさん出ている(過剰発現)ものがあります。こういうタイプのがんは、ホルモン療法が効かないタイプの乳がんに多く、過剰な増殖命令が出てどんどん増殖するので、がんとしての悪性度が高い、タチの悪い乳がんと言われていました。
強陽性が適応
ところが、トラスツズマブが開発されて、状況は一変しました。トラスツズマブはHER2受容体にとりつき、HER2受容体に作用物質が結合するのをブロックします。その結果、細胞に増殖命令が出なくなるのです。トラスツズマブが結合することで、免疫細胞もがん細胞を認識しやすくなり、攻撃をはじめます。こうして、がん細胞は生き残ることができなくなります。
トラスツズマブの適応になるのは、HER2タンパクがたくさん発現している「強陽性」の人です。検査には、がんの組織を染色して調べる免疫組織学染色法と、HER2遺伝子を見るフィッシュ法があります。染色法では、0から+3まで4ランクに分けられ、+3ならば問題なく強陽性で、トラスツズマブの適応です。+2の場合は、さらにフィッシュ法で調べ、HER2遺伝子が増殖していればトラスツズマブの適応になります。
分子標的治療薬の効果と副作用
術後の再発予防にも効果
HER2受容体が強陽性で、分子標的治療薬・トラスツズマブの治療対象になる人は、乳がんの人の20%ぐらいと言われています。
トラスツズマブが日本で乳がん治療に使われるようになったのは、2001年です。当時、健康保険でトラスツズマブの使用が認められていたのは、再発・転移した乳がんに限られていました。しかし、2005年5月には手術後の再発予防にも大きな効果があるというデータが発表され、現在は手術後の再発予防(術後補助療法)にも使われています。
特に、抗がん剤と組み合わせて使うと効果が高いことがわかり、タキサン系の抗がん剤と併用したり、アンスラサイクリン系の薬で治療をしたあと、トラスツズマブを投与するといった方法で治療が行われています。
トラスツズマブは、3週間に1回点滴で投与します(毎週投与する方法もあります)。これを1年間つづけるのが標準的です。
トラスツズマブによる術後補助療法の対象は、HER2タンパクが強陽性の人で、1cm以上の大きさの浸潤がんの患者さんと当初は考えられていました。しかし今では5mm~1cmの大きさの浸潤がん患者さんもその対象と考えられています。
トラスツズマブの副作用
トラスツズマブには、脱毛や悪心@おしん@、嘔吐、白血球の減少など、これまでの抗がん剤に見られたような副作用はほとんどありません。
しかし、投与後数時間から24時間以内に、多くの患者さんに発熱と悪寒@おかん@が見られます。最初は40%ぐらいの患者さんに起こりますが、2回目以降は5%以下と、ごく少なくなります。なぜ発熱や悪寒が起こるのか、その原因はまだわかっていません。
重い副作用として注意が必要なのは、心臓への影響です。トラスツズマブは心臓機能の低下を起こすことがあります。そのため、同じように心臓に影響があるアンスラサイクリン系の抗がん剤とは同時併用しない方がよいと考えられています。また、治療中は定期的に心臓の検査をすることが必要です。
トラスツズマブが登場したおかげで、かつて増殖が早く、ホルモン療法もきかない難しいがんといわれていたHER2陽性乳がんは、むしろコントロールしやすいがんというようなイメージに変わりました。
これは、転移再発した場合でも同様です。再発転移の場合は、ラバチニブというチロシンキナーゼ阻害剤に属する分子標的治療薬も認可されており(転移再発がんの項参照)、さらに現在開発中の薬としてはネラチニブ、ペルツズマブ、T-DM1など目白押しとなっています。しかし、こうした進歩のかげで、最後に残されたのがトリプルネガティブという、ホルモン療法もトラスツズマブも効かないがんです。
(※トラスツズマブの作用メカニズムイラスト)
[コラム] 薬物療法にかかる費用
乳がんの治療費は、手術費用だけでは済みません。術後補助療法は長期にわたるので、その分費用もかかります。
一般的に、3割負担で以下のような費用がかかります。(実際には高額医療費の補助制度もあるため、負担額の計算は複雑です)
●手術後の放射線治療は10万円ほど
●タモキシフェンによるホルモン療法は5年間で20万円ほど
●LH-RHアゴニストは2年で36万円ほど
●アロマターゼ阻害薬は、5年間で30万円ほど
●抗がん剤の場合、6カ月で20万~30万円ほど
●トラスツズマブは、1年間で70~80万円ほど
新薬や分子標的治療薬は薬価が高く、患者さんの大きな負担になっています。このほか、診察代などもあるので、経済的な問題があれば、まず病院のソーシャルワーカーに相談してみましょう。
[コラム] 残された「トリプルネガティブ」
乳がん治療では、エストロゲンやプロゲステロンの受容体があればホルモン療法、HER2受容体がたくさんあればトラスツズマブ、という分子標的治療薬が使われます。
がんそれぞれが持つ個性に狙いをつけて薬物療法を行うわけです。それによって、効かない方への治療を避け、効果の期待できる方に対象を絞って治療を行います。
ところが、ホルモン受容体が陽性の人は7割、HER2受容体が過剰発現の人は2割に限られています。両方陽性の乳がん(ルミナルB/ルミナルHER2タイプ・○ページ参照))もあります。反対に、どちらも陰性で、ホルモン療法の対象にも分子標的治療薬の対象にもならないという人もいます。これが、「トリプルネガティブ」(ホルモン受容体2種類とHER2受容体で3種と数える)と呼ばれるタイプです。
この場合、効果が期待できるのは現在のところ抗がん剤だけになります。抗がん剤の効果は高いタイプですが、がんの特性に狙いをしぼって攻撃できないのが、ネックです。
しかし、トリプルネガティブ乳がんの対策は現在のがん領域の最優先課題の一つでもあり、多くの研究者がかかわっています。トリプルネガティブ自体も、ベイサルライクやクラウディンロウなどのいくつかのサブタイプに分類されることがわかってきました。また、トリプルネガティブに的@まと@をしぼったPARP阻害剤という分子標的薬の開発が進行しています。中でもイニパリブという薬剤が第2相試験(がんを縮小させる効果を見る試験)で有意な効果を示し期待されていましたが、第3相試験(延命効果を見る試験)では全体としての有効性は示せませんでした。紆余曲折は予想されますが、PRAP阻害剤が、必ずトリプルネガティブ乳がんの現在の局面を打開してくれると多くの専門家が期待しています。
月別アーカイブ:
年別アーカイブ:
入院前に準備しておきたいこと
入院前の準備
乳がんの治療法は手術、放射線療法、ホルモン療法、化学療法の4つが基本となり、がんの進行度や性質、患者側の条件により治療法を選択します。手術の入院期間は6日から10日間程度が一般的で、それ以外の治療は原則外来で行います。
治療開始の時期
治療開始はできれば1カ月以内に
乳がんには、早い段階で全身転移をするタイプのものもありますが、一般的には比較的ゆっくり進行するがんです。ですから納得いく治療法を選択する時間的余裕はあると考えられています。ただそうはいってもがんは進行性の病気のため、治療開始が遅れることの不安をだれも否定することはできません。できれば、診断がついてから1カ月以内に治療を開始したいものです。ただ設備の整った病院ではそれなりの手術待ちの時間があるため、早めの意思決定も必要となります
針生検や細胞診のためにしこりに針を刺すと、がん細胞が飛び散ったり転移するので、針を刺したら直ちに手術をしないといけないといわれることがあります。しかしこの説にはさほど根拠がなく、あまり気にする必要はないと思います。むしろ針生検によって病理組織学的診断やホルモン受容体、Her2、核異型度、組織異型度などを事前に把握して治療にのぞむことが現在では主流になっています
ところで治療はまず手術を行うのが普通ですが、抗がん剤治療を先に行う場合も増えています(術前化学療法)。腫瘍が大きい場合や、明らかなリンパ節転移がある場合は積極的に術前化学療法が行われています。具体的には外来で抗がん剤を3週間に1回の割合で4サイクル~8サイクル行うことが一般的で、80%以上の奏効率が期待できます。
最近の早期乳癌の代表的な手術(アクセス制限あり)
ログイン情報はこちらへお問い合わせください
治療に専念できるように環境を整える
仕事を持っている人や幼い子どもを育てている人にとって、乳がんの治療のために何日くらい休みをとればいいのかは、予め知っておきたいことです。 手術のために必要な入院日数は、手術の方法や病院によっても異なりますが、通常10日以内です。しかしその後の治療法の決定は手術結果が判明してからになるので、残念ながら手術前から治療スケジュールを決めることはできません。手術結果によっては再手術が必要になることもあり、治療の順番も放射線が先になったり、抗がん剤が先になったりするからです。手術結果、すなわち切除した組織の病理検査の結果がすべて判明するのに10~14日程度かかるので、この時点で治療スケジュールが決まることになります。
放射線治療や抗がん剤の投与は、一般には通院しながら行いますが、抗がん剤の投与後は、疲れたり気分が悪くなるなどで、数日寝込んでしまう人もいれば、案外平気に活動できる人もいます。
多くの方の場合、術後すぐにでも事務的な仕事なら可能と思いますが、通勤ラッシュや長時間の通勤は辛いかもしれません。また退院後の治療スケジュールも不確定なため、入院期間も含めて1カ月程度の休暇はとっておきたいところです。退院後も放射線治療や抗がん剤投与のための通院の可能性が高いので、そのことも職場の責任者に説明しておき、必要なときに休みをとれる準備をしておきましょう。
家事は、退院後すぐから可能ですが、最初は家族に分担してもらいながら、徐々に元に戻していくようにしましょう。母親や姉妹など、気兼ねなく頼める人がいるようであれば、1週間くらい援助してもらうと、気持ちの上でも楽になります。
入院の費用がどのくらいかかるのかは重要な問題ですが、治療方法、入院日数、差額ベッド代の有無などで変わってきます。気がかりな点は遠慮なく質問して、気持ちよく治療に臨めるようにしましょう。 また、入院申し込み書、手術の同意書、誓約書、健康保険証などの必要書類、病院に持ち込む品物については、印刷物を渡されることが多いでしょう。入院中に必要な品物は、洗面用具や衣類などですが、大きな病院であれば、たいていの必要品は売店にそろえてあります。絶対忘れ物をしてはいけないなどと、神経質になることはありません。
月別アーカイブ:
年別アーカイブ:
乳房温存療法の手術方法
乳房温存療法(Breast-Conserving Therapy: BCT)は、乳癌の治療法の一つで、腫瘍部分のみを切除し、乳房全体を残す手術を基本としています。この治療法は、乳癌による身体的・心理的影響を軽減することを目的とし、広く採用されています。以下に、乳房温存療法の概要、適応基準、治療方法、手術後のフォローアップ、合併症やリスク、再発予防のための工夫などについて詳細に説明します。
1. 乳房温存療法の概要
乳房温存療法は、乳房の外見と機能を保ちながら、癌の根治を目指す治療法です。通常、腫瘍とその周囲の正常組織を切除し、その後、放射線療法を組み合わせることで局所再発を予防します。乳房温存療法の普及により、患者のQOL(生活の質)が大きく向上することが確認されています。
乳房温存療法の目的
乳癌の治療では根治を目指すとともに、乳房の外観を維持し、患者の心理的負担を軽減することが重要です。乳房温存療法はこれらの目的を達成し、乳房切除と比較して治療後の生活における身体的・精神的な満足度が高いとされています。
BCTと放射線療法の組み合わせ
乳房温存療法は通常、放射線療法と併用されます。手術によって腫瘍を除去した後に残った微小な癌細胞を除去するため、放射線治療が行われることで局所再発率を下げる効果があります。放射線治療を併用することで、乳房温存療法を行った患者と乳房全摘手術を受けた患者との間で生存率に大きな差がないことが示されています。
2. 乳房温存療法の適応基準
乳房温存療法は、すべての乳癌患者に適応されるわけではなく、いくつかの基準があります。主に腫瘍の大きさ、病変の広がり、患者の体型や乳房の大きさなどが関係します。以下に適応基準を示します。
適応基準
- 腫瘍の大きさ: 腫瘍が小さく、乳房に対して相対的に大きくない場合に適応されます。通常、腫瘍径が3cm未満であれば乳房温存療法が検討されます。
- 腫瘍の位置: 乳房内の腫瘍の位置も考慮されます。例えば、乳頭近くや乳房の中心部にある場合、切除後の乳房の形状や機能を損なう可能性があるため、慎重に判断されます。
- リンパ節転移: 腋窩リンパ節に転移がある場合、リンパ節郭清や放射線治療が併用されることで乳房温存療法が可能になることがあります。
- 他の医学的条件: 放射線治療を受けられるかどうかも重要です。例えば、放射線アレルギーや既往歴のある場合は、乳房温存療法が適応外となることがあります。
3. 乳房温存療法の手術方法
乳房温存療法では、腫瘍を周囲の正常組織ごとに切除する「部分切除(乳房部分切除術)」や「腫瘤切除術」が行われます。手術方法の選択は、腫瘍の大きさ、形状、乳房内の位置、患者の希望などを考慮して決定されます。
部分切除(乳房部分切除術)
乳房部分切除術では、腫瘍とその周囲の正常組織を数ミリメートルのマージンをもって切除します。この切除範囲を「安全マージン」と呼び、癌の再発を防ぐために設定されます。切除後は、病理検査でマージンに癌細胞が含まれていないか確認します。
腫瘤切除術
腫瘤切除術は、腫瘍の存在する部位のみを切除する方法です。主に腫瘍が小さく、周囲に広がっていない場合に適応されます。腫瘤切除後、形状の維持を目的とした乳房再建術が行われることもあります。
4. 手術後のフォローアップと再発予防
乳房温存療法後の再発予防のため、手術後には放射線療法が行われます。さらに、ホルモン療法や化学療法などが組み合わせられることもあります。
放射線療法の役割
放射線治療は、切除後に残存している可能性のある癌細胞を破壊し、局所再発率を低減させます。放射線治療は通常、手術後3〜6週間程度にわたり毎日行われます。
ホルモン療法・化学療法の併用
ホルモン受容体陽性の乳癌患者に対しては、ホルモン療法が行われ、ホルモン感受性のある癌細胞の増殖を抑制します。また、腫瘍の悪性度が高い場合やリンパ節転移が確認された場合には、化学療法が併用されることもあります。
5. 合併症とリスク
乳房温存療法には、いくつかのリスクや合併症が伴いますが、主なものを以下に挙げます。
傷跡や乳房変形
乳房部分切除では、切除後の傷跡や乳房の形状変化が生じることがあります。特に腫瘍が大きい場合には、術後に乳房の変形が顕著になる可能性があります。こうした変形を軽減するために、再建手術が選択されることもあります。
再発リスク
乳房温存療法を受けた患者には、局所再発のリスクがあります。ただし、放射線治療を併用することで、再発リスクはかなり低減されます。また、手術後の定期的なフォローアップや自己検診が推奨されます。
放射線治療による副作用
放射線治療は局所的な影響を及ぼすため、皮膚の炎症や乳房の腫れなどの副作用がみられることがあります。また、稀に肺や心臓に影響が及ぶこともあるため、適切なフォローアップが必要です。
6. 乳房温存療法の将来と患者サポート
乳房温存療法の技術や治療法は年々進化しており、患者にとってさらに良い結果が得られるようになっています。また、患者の心理的ケアも重要視されるようになり、患者支援プログラムが多くの病院で提供されています。
新たな治療法の研究
乳房温存療法では、さらに効果的な放射線療法や、腫瘍をターゲットにした新しい治療法が研究されています。こうした技術の進展により、今後はさらに多くの患者が乳房温存療法を受けることができると期待されています。
サポートプログラムの充実
乳癌患者の心理的負担を軽減するため、サポートプログラムの充実が図られています。患者が自分の治療に対する理解を深め、手術後の生活の質を向上させるために、心理カウンセリングや患者教育が行われています。
まとめ
乳房温存療法は、乳癌治療における重要な手法の一つであり、乳房の外観と機能を保ちながら根治を目指す治療法です。適応基準を満たした患者には、腫瘍の部分切除と放射線療法を組み合わせた治療が行われ、乳房全摘術と同等の生存率が期待されます。手術後のフォローアップや心理的支援も重要で、患者のQOL向上に大きく寄与しています。
2024年10月記載
——————————————–
手術――乳房温存療法の手術方法
乳がんの手術には乳房を残す乳房温存手術と乳房を全摘してしまう乳房切除手術があります。また乳房温存手術といっても切除範囲を狭くするか、広くするかによって術後の印象は随分ちがってきます。
Ⅰ~Ⅱ期の乳がんでは乳房温存療法が標準的治療
乳房温存療法とは乳房を部分的に切除して、残された乳房に放射線を照射する治療法です。現在、Ⅰ期とⅡ期の乳がんであれば、7割程度の患者さんが乳房温存手術の適応と考えられています。欧米に比べて日本は乳房温存療法の導入が遅れていましたが、今では乳がん治療の半数程度が乳房温存療法だと推測されます。
乳がんの手術の目的は、がんを確実にとり除くことです。ですから、乳房切除手術のほうがその目的にそっているといえますが、たとえ、乳房内に微小な顕微鏡レベルのがん細胞が残っていたとしても、手術後に放射線を照射することでがん細胞を殺すことが多くの場合できると考えられています。
乳房を温存した場合と切除した場合の比較試験が欧米で行われ、一定の条件を満たせばどちらの方法でもその後の生存率に差はないという結果が得られています。
乳房温存療法がふさわしくない場合も
しこりの大きさや乳がんのステージに関わらず、次の場合には乳房温存療法は好ましくないと考えられています。
・乳房内に石灰化が広汎にひろがっていたり、腫瘍が離れて二つ以上ある。
・手術でとり除いた組織の断端にがん細胞があり、10年以内の局所再発率が高いと判断される。
・妊娠している。
・皮膚筋炎や多発性筋炎などのような膠原病(放射線を照射すると皮膚の反応が強く出る)がある。
・乳房に対して腫瘍が大きい。
・本人が乳房温存療法を望まない。
乳房温存手術の切除範囲
乳房を温存する場合でも、腫瘍を中心に1cm程度の安全域をとりながら比較的小さく切除する方法(腫瘤切除術/ランペクトミー)と乳房の4分の1程度をとってしまう方法(4分の1切除術)では術後の外見的な印象は大きく違ってきます。切除範囲が広ければがんを取り残すリスクは小さくなり、局所再発のリスクも小さくなりますが外見的な印象が悪くなるので、実際には前述した2つの方法の中間的な手術が多くの場合行われています。どちらに近い手術をするかは、がんのひろがりなどの条件とともに、患者側の希望も重要ですから、希望事項はあらかじめ主治医に伝えておくといいでしょう。
ハルステッド法 乳がんの手術は長い間、乳房、大胸筋、小胸筋、腋窩リンパ節をすべて切除するハルステッド手術が標準治療とされてきました。1970年代末になって大胸筋を温存する手術でも生命予後に差のないことがわかってきました。現在では、大胸筋にがんが直接浸潤している場合は筋肉を切除することもありますが、いわゆるハルステッド手術は行われていません。
手術――乳房温存療法でのがんの取り残し
乳房温存療法では安全域をつけて手術をしても、取り残しの可能性があります。残った乳房に放射線を照射することで、局所再発率を低下させることができます。
乳房温存療法では放射線照射が必須
前述したとおり、乳がんの手術の目的はがんを確実にとり除くことです。そのために、乳房温存療法ではしこりの部分に安全域をつけて切除するわけですが、それでも、がんを完全に取り除けたかどうか、手術の時点ではわかりません。マンモグラフィーやエコー、MRIなどの術前検査では発見できない微細ながんが残っている可能性がありうるのです。
そこで、切除した組織の断端を、顕微鏡でがんがないかどうか調べます。そこにがんがなければ、がんをとりきれている可能性は高くなりますが、がんのすべてが連続して広がっているわけではありません。細かく検査をすれば見落としは減らせますがゼロにはなりません。断端にがんがあった場合は、手術後の乳房内の局所再発率が高くなりますが、がんがないと判断された場合でも、手術だけでは40%くらいの確率で局所再発するというデータもあります。
乳がんは放射線に対する感受性が高いので、乳房に放射線をかけることで微細ながんを死滅させることができます。放射線照射により、局所再発率はかけない時の4分の1にまで低下するといわれています。このため乳房温存療法は放射線照射とセットの治療法であると考えるのが一般的です。
取り残しがあるときは再手術
手術によって切除した組織の断端にがんが見つかった場合、原則として再手術をすることになります。その際、乳腺に余裕があればもう1度乳房を温存する方法も可能です。この場合も、再度切除した断端にがんがあるかどうかの病理検査を行い、それでがんがみつからなければOKということになります。乳房をかなり大きく切除し、これ以上取ると美容的に乳房を残す意味が薄れる程度まで切除したにも関わらずがんが断端に残ってしまうような場合は乳房の全摘が勧められます。ただ断端陽性でも放射線をかけることで案外再発しないこともあり、リスクを承知で乳房を残すこともひとつの選択肢にはなりますが、その場合は全摘、乳房再建という別のアプローチとの比較検討がなされます。
がんは局所再発しても生命予後は変わらない?
誰だって、手術を受けた乳房内に乳がんが再発して平然としていられるわけはありません。たとえ局所であっても、再発=命とりと考えてしまいがちです。ただ、局所再発については、その後の生命には影響しないという考え方もあります。 がんで死亡するのは、ほとんどが遠隔転移によるものです。乳がんには早い段階から遠隔転移するものがありますが、遠隔転移するかしないかは、がんとその患者さん個人の免疫の力関係で決まることで、局所再発は生命を左右しないというのです。そして、がんが発見された時点では、遠隔転移するようながんはすでに転移を起こしているので手術方法は予後を左右しないという考え方も成り立ちます。 一方局所再発した乳がんが新たに転移する能力を獲得することもないとはいえません。最初はおとなしい乳がんだったのに時間的な経過とともに悪性度を増すことをまったく否定することはできません。ですから、局所再発を過剰に恐れるのもこれまでのデータからみて適切ではありませんが、極力局所再発を防ぐ努力をしたほうが無難だと考えられています。
月別アーカイブ:
年別アーカイブ:
乳房温存療法でのリンパ節の治療
手術――乳房温存療法でのリンパ節の治療
乳房切除手術でも乳房温存手術でも腋窩リンパ節をとり除くことが原則でした。ただ、最近は最小限のリンパ節を切除するだけですむ手術法が普及しつつあります。
リンパ節は有害物をとり除くフィルター
人体には血管とは別に、体液の流れであるリンパ管のルートがあります。リンパ管も血管と同様に全身に張りめぐらされていますが、体の要所要所にあるリンパ節で細菌やウイルスなどの有害物や老廃物質をキャッチして排除しています。リンパ節はフィルターの役目をしているわけです。
乳房内にもリンパ管が網の目のようにはりめぐらされています。がん細胞も有害物の一つで、リンパの流れにのって、リンパ節へ運ばれていきますが、ここでキャッチされて排除されます。しかし、排除しきれないと、リンパ節ががんに乗っ取られた状態になり、この状態がリンパ節転移だと考えられています。
乳がんでは、その多くが乳房に隣接する腋窩リンパ節へ最初に転移しますが、一部は胸の中央にある胸骨傍リンパ節へ転移します。
腋窩リンパ節郭清の有無は生存率に影響しない?
長い間、乳がんの手術では、乳房切除手術でも乳房温存療法でも腋窩リンパ節を郭清していました。郭清とは、リンパ節を周囲の脂肪組織ごとすべて除去することです。
乳がんに限らず、がんはまず近くのリンパ節に転移し、そこからさらに次のリンパ節というようにリンパ節転移を繰り返した後、血液に入りこんで全身転移を起こすと昔は考えられていました。長年、乳がんの標準的治療とされてきたハルステッド手術も、この考え方に基づいて行われてきました。リンパ節の郭清は、全身転移を防ぐ上での水際作戦と考えられていたのです。
また、以前は、乳がんが発見された時点ですでにリンパ節転移が起こっていることが多く、リンパ節を郭清することは局所をコントロールする上で必須の処置ともいえました。
しかし、リンパ節を郭清することは、その場所でリンパの流れが途切れることになりますから、腕がむくむことがあり、それが患者さんのQOLを損なうといった問題を生じます。
その後、診断技術の進歩により乳がんが早期で発見される率が高くなると、腋窩リンパ節への転移のないケースもふえてきました。そこで、術前検査でリンパ節に転移がなさそうな場合には郭清が不要なのではないかという考え方が出てきました。データからはリンパ節を郭清することが、生存率のアップにつながっていないこともわかってきました。
センチネルリンパ節生検法とは
乳房内のしこりのサイズだけで、リンパ節への転移が起こっているかどうかは判断できません。あきらかに、リンパ節がしこりになっているなどの場合は転移があると予想できますが、しこりとして触れないから転移していないとは限らないのです。手術でリンパ節を切除して調べた結果、はじめて転移の有無がわかるのです。
しかし、乳がんのリンパ節への転移は無秩序に起こるのではなく、一定の道筋のあることが最近わかってきました。リンパ節のサイズは直径数㎜から1㎝くらいで、大豆に似た形をしています。それがわきの下には20~50個くらいありますが、がんが乳房内のリンパの流れに乗って、最初にたどり着くリンパ節は決まっているらしいということがわかってきたのです。とすると、がんが最初にたどり着くリンパ節に転移が起こっていなければ、ほかのリンパ節は切除して調べるまでもなく、転移していないと考えられます。このような考え方に基づいて登場したリンパ節の手術法がセンチネルリンパ節生検法です。
急速に普及しているセンチネルリンパ節生検法
センチネル(sentinel)とは、見張りとか前哨という意味です。つまりがんの侵入を見張っているリンパ節と考えたらいいでしょう。
では、20~50個ある腋窩リンパ節の中で、どれがセンチネルリンパ節なのかということが問題になりますが、それを調べるためにアイソトープや色素が用いられています。がんの周囲にアイソトープや色素を注入して、それらが最初に流れこんだところがセンチネルリンパ節というわけです。アイソトープと色素の両方を用いる場合と、どちらか一方だけを用いる場合があります。
センチネルリンパ節を見つけたら、それを摘出して調べ、転移がなければそれ以上のリンパ節切除は必要ないということになります。この方法で実際に転移したリンパ節を見落とす率は手術対象者全体の2%以下と考えられています。
センチネルリンパ節生検法は患者さんへの負担も少なく、リンパの流れが滞らないので、治療後、腕のむくみの起こる心配もあまりありません。ただし、センチネルリンパ節生検法の先進国であるアメリカでさえ登場してまだ10年程度です。今後、長期にわたって、リンパ節を郭清した場合と比較して生命の予後に差はないか、局所再発率はどうかなどまだ不明と点も多くあります。技術的にもリンパ節の発見法、発見したリンパ節の検査法、微小転移の扱いなど未解決の問題も多くあります。 このように、センチネルリンパ節生検法は多くの問題点をかかえながらもその後遺症の少なさが評価され、アメリカではすでに標準治療といっていい普及状況になっており、日本でも都内の主要施設に関していえば標準治療という状況にあります。
月別アーカイブ:
年別アーカイブ:
非定型的乳房切除手術
非定型的乳房切除手術(Non-standard Mastectomy)は、一般的な乳房切除手術とは異なる手法や適応を持つ乳房の外科的切除方法を指します。通常の乳房切除手術は、乳がん治療の一環として行われ、がん細胞が再発するリスクを抑えるために、乳房全体や一部を取り除く手術が一般的です。しかし、非定型的な手術は患者の病状や個々の希望、あるいは医療チームの判断により、より特殊な方法で行われる場合があるため、異なる手術手法や適応範囲が含まれます。
以上、2024年10月記載
手術――非定型的乳房切除手術
乳房を全て切除する手術です。腋窩リンパ節は郭清しますが、大胸筋は残せるので、胸がえぐれることはありませんし、腕も普通に動かせるようになります。
通常は大胸筋も小胸筋も残す
乳房温存療法が適応できないとき行われる手術の中での標準的な手術法が非定型的乳房切除手術と呼ばれるものです。リンパ節の郭清は行いますが、大胸筋は残します。長い間、大胸筋も小胸筋も切除するハルステッド手術が標準的治療法(定型的乳房切除術)であった歴史的経緯から、このような名前で今も呼ばれています。
小胸筋については、切除する方法と残す方法がありますが、通常は大胸筋も小胸筋も残す方法が行われています。
最近はひどく進行した段階で乳がんが発見される率は少なくなっていますが、中には大胸筋まで広範囲にがんが浸潤しているケースもあります。その場合には、大胸筋の切除も行われることになります。結果としてハルステッド手術と近い手術法になることもゼロではありませんがいわゆるハルステッド手術は過去の遺物といえる状況になっています。
なお乳房切除をする場合でもリンパ節転移の可能性が少ないと予想される場合はセンチネルリンパ節生検を行なって、腋窩リンパ節郭清を省略する試みも最近は始まっています。
抗がん剤の投与で乳房温存が可能になる例も
乳房内に広汎に微小石灰化があるときや、切除した組織の断端にがんがどうしても残る場合は乳房温存療法ができないため、乳房切除手術をすることになります
がんが大きいときも、切除する範囲が広くなるので、乳房を温存したとしても、残される乳房が美容的ではないため、乳房切除を行い、そのあと乳房を再建したほうがよいと考える人も多いことでしょう。
しかし、発見したとき、すでにⅡ期の後半やⅢ期で、がんが大きい場合であっても、先に抗がん剤を投与することによって、がんを小さくすることが多くの場合可能です。ですから、単純にしこりが大きいために乳房温存が不向きな場合は術前抗がん剤という方法によって乳房を残せる場合も少なくないので、主治医と相談して乳房を温存する可能性をさぐってみてもよいでしょう。
月別アーカイブ:
年別アーカイブ:
センチネル(見張り)リンパ節生検
乳腺の組織にはリンパ管がネットワーク状に張りめぐらされており、乳腺内に発生した異物などはこうしたリンパ管を通じて、腋窩にある見張りリンパ節(センチネルリンパ節)に注ぎこまれます。ここからさらにリンパ節がネットワーク状に分布されており(腋窩リンパ節)、生体にとっての異物が処理されていきます。このため乳房に発生したがん細胞もリンパ管を通じてセンチネルリンパ節に集められ、さらにそこから周囲のリンパ節にも運ばれ処理されます。リンパ節ががん細胞を処理できれば問題ありませんが、処理しきれなければ転移が成立します(リンパ節転移)。このためセンチネルリンパ節に転移があれば他のリンパ節にも転移がある可能性が高く、センチネルリンパ節に転移がなければ他のリンパ節はまず大丈夫と考えられます。このような考え方は、【センチネルリンパ節の仮説】と呼ばれ、かなり真実に近いと思われています。 今日の乳がん治療の論点のひとつに腋窩リンパ節をどのように取り扱うかという問題があります。
腋窩リンパ節郭清(伝統的な方法)
転移の可能性のある腋窩リンパ節(小胸筋の内縁まで)を完全に(系統的に)切除する方法で通常10~30個程度のリンパ節が切除されます。
○腋窩リンパ節転移の有無の診断および治療(局所コントロール)のためには最も確実な伝統的方法です。
×合併症として、上肢のむくみ、腋の違和感、感覚低下などが一定の頻度で起こります。他覚的な上肢のむくみの発生頻度は10~20%程度とされています。
乳房内に注入されたアイソトープと同定されたセンチネルリンパ節(リンフォシンチグラフィー)
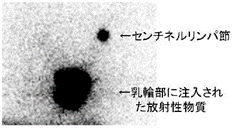
センチネルリンパ節生検(新しい方法)
色素や放射性物質を腫瘍の周囲または乳輪部に注入し、その物質が最初に注がれるリンパ節(センチネルリンパ節/通常1~2個=最も転移がみつかる可能性の高いリンパ節)だけを見つけ切除する方法。術中の迅速病理診断で転移が見られれば、腋窩リンパ節郭清に切りかえます。 現在都内の主要施設では適応のある患者さんにとっての第一選択の治療であり、伝統的なリンパ節郭清を最初から選択することは少なくなっています
後遺症が非常に少ない方法です。腕のむくみはまず起きないとされています。
虎の門病院でのセンチネルリンパ節生検法の実際について
1)RI法と色素法の併用法で行う場合と色素法単独で行う場合があります
RI法 使用するトレーサー 99mTc‐フチン酸
ガンマプローブ Navigator
色素法 使用する色素 インジゴカルミンまたはパテントブルー
2)全身麻酔で乳房の手術と一緒に行う場合が一般的ですが、術前に化学療法を行う方は局所麻酔でリンパ節生検だけを行う場合があります
3)リンパ節の病理検索はホルマリン固定後2mm全割にて検索します。術中迅速診断にて転移ありと診断されれば、リンパ節郭清をその場で追加します。免疫染色での検索は組織型などの要因により追加します。
A;対象となる方の条件
A-1 あらかじめ腋窩を触診、超音波、CT等で検索しリンパ節転移の疑いがないことが第一条件となります。
A-2 しこりがかなり大きい人の場合はリンパ節に転移している可能性が高いため(検査前確率が高いという表現をします)除外したほうが無難とされています。
A-3 乳房温存手術、乳房全摘手術に関わらず、センチネルリンパ節生検の対象としています。
B;手技の概要
センチネルリンパ節生検法(RIと色素法の併用の場合)
前日にRIを乳輪部に注入し、リンフォシンチグラフィーの撮影を行います。手術時に色素を乳輪部または腫瘍の周囲に注入し、色素で染まるリンパ節(1~2個/センチネルリンパ節)を見つけ切除します. 同時にガンマプローベで放射性物質が取り込まれていることを確認します。切除したリンパ節は迅速病理組織検査を行う場合と、そのままホルマリン固定する場合があります。
術中迅速診断にてリンパ節転移が確認されれば、腋窩リンパ節郭清(レベル1,2)に切りかえます
切除されたリンパ節は術後さらに永久標本で検査を行い(2mm全割)転移の有無を詳しく検査します。必要に応じて免疫染色を追加します。その結果リンパ節に転移が発見された場合は、後日再手術による腋窩リンパ節郭清(レベル1,2)または腋窩の放射線照射を行います。
以上のようにセンチネルリンパ節生検法は従来の手術と比較して後遺症の少ない方法です。
乳房部分切除+センチネル生検+乳房照射50Gy治療後
【実臨床でのセンチネルリンパ節生検の腋窩制御率について】
虎の門病院乳腺内分泌外科データ
<背景>’90年代末より、乳癌の実臨床において導入されたセンチネルリンパ節生検(SLNB)は徐々に浸透し、’00年代半ばにはN0乳癌の標準的術式として扱われるようになった。海外で実施された無作為化臨床試験の結果を踏まえ、SLNにmicro転移を認める症例、さらにはmacro転移を認める症例に対する腋窩郭清省略が実臨床でも取り入れられつつある。今回腋窩治療の諸問題を議論するにあたり、当院での’00年代後半の症例をレトロスペクティブに検討した。
<対象と方法>当院で2006年9月から2009年12月までにSLNBを施行した513例を検討の対象とした。 同定法は色素、RIの併用で行い、T2以下のN0症例は原則SLNBを行い、またSLN転移陽性例には原則郭清を実施した。513例の内訳はTis 61、T1 279例、T2 159例、T3 14例であった。
<結果>SLN転移陽性例はTis 0/61(0%) T1 48/279 (17.2%) T2 49/159 (30.8%) T3 6/14(42.9%) であり全513例中103例(20.1%)に微小転移以上の転移を認めた。SLN陽性例のうち2個以上の転移を認めたものはT1 16/48(33.3%) T2 21/49(42.9%) T3 3/6 (50%) 計40/103(38.8%)であった。SLN転移陽性例のうちnon-SLNにも転移を認めたのはT1 13/48(27.1%)、T2 14/49(28.6%)、T3 3/6(50%) で計40/103(29.1%)であった。このうちACOSOG Z-0011試験適格例(T1又はT2、乳房温存例、SLN転移2個以下、)は57例で、このうち13例にnon-SLNに転移を認め(22.8%)、この割合はZ11試験の結果をはじめ諸家の報告に近い。
これら513例のうち、フォローアップが可能であった495例(平均観察期間5.0年)について、乳癌再発を17例(3.4%)に認め、他癌21例、癌以外の他病死2例であり、これらを合わせたevent を39 例(7.8%)に認めた。乳癌再発17例中11例に遠隔再発を認め、腋窩再発は4例(0.8%)であったが、腋窩単独再発が2例(0.4%)、胸壁、腋窩再発1例、遠隔再発に腋窩再発を伴うものが1例であった。この4例はいずれも初回手術でSLN転移陰性例であった。SLNBにて転移を認めた103例に関して、乳癌再発3例(遠隔2例、乳房内再発1例)を認め、他癌4例(卵巣癌2例、肺癌1例、皮膚癌1例)を認めたが、腋窩再発は認めなかった。
<結語>SLNB適応例の腋窩制御率が99%以上で、他癌の罹患率が4.2%である現実を踏まえると、腋窩治療の方法が、患者の生存率に対して現実的なインパクトを与える可能性は少なくQOL改善を念頭においた術式の採用が妥当と思われる。
月別アーカイブ:
年別アーカイブ:
乳房再建手術について
乳房再建手術について
1. はじめに
乳房再建手術は、乳がんの治療やその他の理由で乳房を部分的または完全に失った患者に対し、失った乳房を外科的に再構築する手術です。乳房再建は、身体的な外見の回復だけでなく、患者の心理的な回復にも大きく貢献します。近年、乳がんの治療法や技術の進歩に伴い、乳房再建手術の選択肢も増え、患者が自分に合った方法を選ぶことができるようになりました。本稿では、乳房再建手術の概要、手術方法、タイミング、メリット・デメリット、そして手術後のケアについて解説します。
2. 乳房再建手術の概要
乳房再建手術は、乳房切除(乳房全摘)や乳房部分切除(乳房温存手術)後に、乳房の外観を再構築することを目的とした外科手術です。この手術には主に2つの方法があり、「インプラント法」と「自家組織移植法」があります。患者の身体状態や治療計画、希望に基づき、これらの方法の中から最適な選択肢が選ばれます。
再建の目標は、自然な形状の乳房を作り出し、患者が見た目や自尊心を取り戻す手助けをすることです。また、再建により身体のバランスが整い、服装の選択肢が広がるなど、生活の質の向上にも寄与します。
3. 再建手術のタイミング
乳房再建手術は、乳がんの治療計画に応じて、2つのタイミングで行われます。
3.1 同時再建
乳房切除手術と同時に再建手術を行う方法です。患者が乳房を失うショックを軽減するため、乳がん手術後すぐに乳房の再建が行われるため、心理的な負担が軽減されることが多いです。また、皮膚や乳房の形状が保たれるため、再建の結果が自然になる場合が多いのが特徴です。
3.2 二期再建
乳房切除後、一定の治療期間を経てから再建を行う方法です。特に、放射線治療が必要な患者や、全身の健康状態が十分でない患者に選択されることが多いです。放射線治療が行われると、皮膚や組織の質が変化し、再建に影響を与える可能性があるため、治療が完了してから再建を検討します。
4. 乳房再建の方法
乳房再建には主に2つの方法があり、患者の身体の状態や希望に応じて選ばれます。各方法にはそれぞれのメリットとデメリットがあるため、医師と十分に相談することが重要です。
4.1 インプラント法(人工乳房)
インプラント法は、シリコンインプラントや生理食塩水インプラントなどの人工物を使用して乳房を再構築する方法です。この方法は、比較的手術が簡便で、回復も早いという利点があります。主に以下の2つの手術ステップがあります。
- エキスパンダー挿入: 乳房切除後、乳房皮膚や筋肉の下に「ティッシュ・エキスパンダー」と呼ばれる伸縮性のある袋を挿入し、皮膚を徐々に伸ばしてスペースを確保します。このエキスパンダーは、数週間から数か月間にわたって生理食塩水を注入し、徐々に膨らませていきます。
- インプラント挿入: エキスパンダーで皮膚が十分に伸びた後、最終的なインプラント(シリコンや生理食塩水でできたもの)を挿入して乳房を形成します。
インプラント法は手術時間が比較的短く、体の他の部位から組織を採取する必要がないため、体への負担が少ない点が魅力です。しかし、インプラントは数年ごとに交換が必要になる可能性があるほか、感染やカプセル拘縮といった合併症のリスクも存在します。
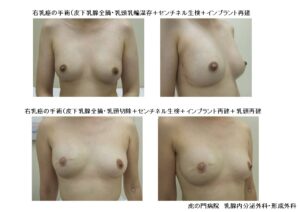
乳房再建(インプラント)
4.2 自家組織移植法
自家組織移植法は、患者自身の体の別の部分から皮膚や脂肪、筋肉などの組織を移植して乳房を再構築する方法です。一般的に使用される組織には、腹部、大腿部、背中の筋肉などがあります。この方法は、見た目や手触りが自然に仕上がることが多く、長期的な維持が可能である点が利点です。
- 腹直筋皮弁法(TRAM法): お腹の皮膚、脂肪、筋肉を使って乳房を再建する方法です。この方法では、余分な腹部脂肪を利用できるため、腹部のシェイプアップ効果も期待できます。
- 遊離皮弁法(DIEP法): 腹部から皮膚や脂肪を採取する方法ですが、筋肉を使用しないため、術後の機能的な影響が少なくなります。
- 広背筋皮弁法: 背中の皮膚、筋肉、脂肪を移植して乳房を再建する方法です。この方法は、背中の組織が比較的しっかりしているため、インプラントと併用することもあります。
自家組織移植法は、自然な見た目と感触を得られることが多い反面、手術が複雑で時間がかかり、体の別の部分に大きな切開を必要とするため、術後の回復に時間がかかるというデメリットもあります。
5. 再建手術のメリット・デメリット
乳房再建手術には多くのメリットがありますが、デメリットやリスクも存在します。患者はこれらを十分に理解し、医師とよく相談した上で手術を決定することが重要です。
5.1 メリット
- 外見の回復: 乳房を再構築することで、手術前の外見を取り戻すことができ、衣服のフィット感も改善します。
- 心理的な効果: 再建手術により、身体のバランスが整い、自尊心の向上や精神的な安心感を得られることがあります。
- 生活の質の向上: 乳房再建により、日常生活の中での不便さや身体的な違和感が軽減され、患者の生活の質が向上します。
5.2 デメリット
- 合併症のリスク: インプラント法では、カプセル拘縮や感染、インプラント破損などのリスクがあります。また、自家組織移植法では、移植部位の手術に伴うリスクや合併症が考えられます。
- 手術回数の増加: 乳房再建は一度の手術で完了するとは限らず、数回にわたる手術や調整が必要となることがあります。
- 長期的なメンテナンス: インプラントを使用する場合、経年的なメンテナンスが必要となる可能性があります。インプラントが破損した場合や形状が変化した場合には、再手術が必要です。
6. 手術後のケアとフォローアップ
乳房再建手術後には、適切なケアとフォローアップが重要です。術後の回復期間中は、痛みや腫れ、違和感を感じることがあり、特に自家組織移植法では回復に時間がかかることがあります。
6.1 術後の管理
術後は、感染を防ぐために定期的な消毒やドレーンの管理が必要です。また、術後数週間は無理をせず、医師の指示に従って日常生活を徐々に再開していくことが推奨されます。さらに、術後の経過を確認するために定期的な通院が必要です。
6.2 長期的なフォローアップ
再建乳房の状態を確認するために、定期的なフォローアップが必要です。特にインプラントを使用した場合は、数年ごとに状態をチェックし、必要に応じて交換や修正を行います。また、再発リスクのある乳がん患者の場合は、乳房の再建後も定期的ながん検診が欠かせません。
7. 結論
乳房再建手術は、乳がん治療後の身体的および心理的な回復に大きく貢献する治療法です。インプラント法と自家組織移植法という2つの主要な方法があり、患者のニーズや健康状態に応じて選択されます。再建手術は見た目の回復に留まらず、患者の生活の質の向上にも寄与しますが、手術にはリスクやデメリットも伴うため、十分な情報を基に医師と相談して決定することが重要です。
2024年10月作成

2013年7月から、人工物(インプラント)による乳房再建も保険適応になり、選択の幅がひろがりました
再発発見の遅れは心配ない
最近は、日本でも、乳房温存療法が乳がん手術の半数を占めるようになりましたが、それでもまだ乳房切除術が必要な人が多くいます。こうした人に、ぜひ知っていただきたいのが乳房再建術です。 乳房再建が終わってはじめて乳がん手術が完了する、といわれるほど乳房再建が一般化している国もあります 日本でも、ようやくここ10年ほどの間に乳房再建に対する関心が高まり、再建術を受ける人も少しずつですが増えてきました。乳房再建の技術そのものも、ずいぶん進歩しています。 乳房再建をためらう理由の一つに、「再発の発見が遅れるのではないか」という心配があるようです。しかし、人工乳房(インプラント)を挿入するのは大胸筋の下で、局所再発の場合は、もっと表面の皮膚や皮下に出ます。超音波検査など、体の外から内部の状態を調べられる検査も発達しているので、特にこの方法の場合乳房再建によって再発の発見が遅れる心配はないと考えてだいじょうぶです。
代表的な乳房再建手術
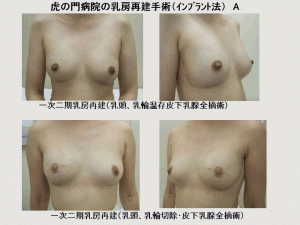
事前に十分吟味して
また、乳房を喪失してつらい思いをするのは、若い人も年配の人も同じです。現実問題として、左右のバランスが悪い、温泉旅行が楽しくなくなった、補整下着をつけるのが面倒、夏でも胸のあいた服が着られないなど、いろいろな不自由を感じることも少なくありません。もう年だから、と再建を恥ずかしがる必要はまったくないのです。 大切なことは、手術を受ける前に十分再建の方法や時期、執刀医の力量などを吟味し、再建後のイメージをある程度つかんでから再建術を受けることです。 再建術を執刀するのは、基本的に形成外科の医師です。患者側の条件にもよりますが、執刀医の力量によっても出来ばえはだいぶ違います。左右ふぞろいで、何のために再建を受けたのかわからない、といったことにならないように、事前に十分基礎的な知識を持って、方法や時期、施設などを選択しましょう。
代表的な乳房再建手術
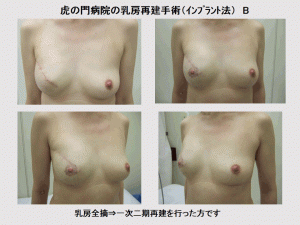
時期と再建の方法に2種類
乳房再建は、再建の時期によって2つに分けられます。乳がんの手術と同時に再建を開始するのが「一次再建」、がんの手術後一定の時間をおいて乳房再建を開始するのが「二次再建」です。さらに、再建に何を使うかで2種類に分類されます。人工乳房(インプラントともいわれ、シリコンバッグなどを使う)を使う方法と、自分の皮膚:皮下組織や筋肉など自家組織を使う方法です。 がん治療で胸に放射線照射を受けているかどうかで、選択肢も大きく違ってきます。まず、こうした条件を一つずつ考えていきましょう。
一次再建か二次再建か
手術回数が少ないのは一次再建
最初に、乳房再建の開始時期を考えてみましょう。 先に述べましたように、がんの手術といっしょに再建術を開始する一次再建と、手術が終わったあとであらためて再建術を開始する二次再建という選択肢があります。 一次再建の利点は、何といっても、自家移植ならば一度に手術が終わってしまうことです。この場合麻酔から覚めたときにはすでに乳房が再建されているので、自分が乳房を失った姿を見ないですむのも利点といえるでしょう。
じっくり考えるなら二次再建
では、一次再建のデメリットは何かといえば、やはり十分に吟味する時間がないことです。特に、自分ががんだとわかったショック、おそらく初めて受ける手術への不安感などで、頭の中はいっぱいだと思います。その先にある乳房再建の問題で、どういう方法を選んだらいいのか、どこの施設や医師に再建術をしてもらったらいいのか、といったことまで考える余裕がない人がほとんどだと思われます。 病理の検査結果が判明していない時点で再建手術を行うことの問題もあります。後でリンパ節転移が多かったとか、切除検体の断端が陽性などの結果がでると対応に苦慮することになります。 また、乳房に局所再発した場合には、切除が基本ですから、せっかく再建した乳房を取り外さなければなりません。そういう意味では、局所再発の危険が高い2年ぐらいは待ってから再建するというのも一つの選択肢です。
放射線照射の有無も問題
もう一つ、放射線照射との関係も考えなくてはなりません。放射線照射は、皮膚にもダメージをあたえます。放射線によって皮膚が萎縮したり繊維化して固くなるので、せっかく再建した乳房も、美容的な意味がなくなることもあります。 乳房切除でも、腋窩リンパ節に4個以上の転移があれば術後に放射線照射を行います。リンパ節転移の数がもっと少ない場合でも放射線照射を行うこともあります。 そのため、放射線照射が行われないと予想される人にしか一次再建はしない方が無難という考え方もあります。 二次再建の場合は、ふつう乳がん手術のあとが落ちついてから、だいたい半年後ぐらいからはじめます。何年たったからもうできないということはありません。再建は、手術から5年後でも10年後でもできます。十分時間をかけて考えてから再建することもできるのです。 ただし、手術が1回余分に必要なことと、一次再建より費用がかかるのが欠点です。 こうした点をよく考えて、医師と相談しながら手術の時期を決めてください。
乳房再建には、2種類あります。
簡単な手術で挿入できる人工乳房
乳房再建は、再建に何を使うかで2つに分かれます。一つは、自分の組織を使う自家移植。もう一つは、人工乳房といって、生理食塩水の入ったバッグや豊胸手術などでも使われるシリコンバッグを埋め込む方法です。
人工乳房を使った再建術
一番簡単に乳房再建ができるのが、人工乳房を使う方法です。 人工乳房には、生理食塩水を入れたバッグとシリコン(ソフトコヒーシブシリコンなど)があります。生理食塩水のバッグは、大きさに合わせて生理食塩水を注入するので、左右の大きさをそろえられるのが利点です。ただ、水なので、乳房とはだいぶ質感が違い、ポチャポチャ音がすることもあります。 現在は、人工乳房といえばシリコンを指しています。これは、乳房とよく似た質感があり、豊胸手術にも使われています。 人工乳房を入れられるのは、胸の大胸筋@だいきょうきん@を残して乳房切除(胸筋温存乳房切除術)を行った人です。したがって、現在は乳房切除を受けた人のほとんどが該当します。
【単純人工乳房挿入法】
中でも簡単なのは、乳房切除後、かわりに人工乳房を入れる方法です。手術で乳房内部の乳腺組織だけを切除し、大胸筋はもちろん、乳房の皮膚や乳頭、乳輪なども残っている場合(乳頭乳輪温存皮下乳腺切除術)には、手術に引きつづいて人工乳房を挿入します。 まず、乳腺組織を摘出した傷からメスを入れ、大胸筋をはがします。その下に人工乳房を入れて、ふくらみを再現します。これは一次再建が基本で、外見的には、比較的元に近いきれいな乳房ができます。アメリカでは比較的人気のある方法ですが、これができるのは十分ふくらみがつくれる皮膚が残っている人に限られます。
【組織拡張法】
乳がん手術は、ふつう皮膚ごと乳房を切除してしまうので、人工乳房でふくらみをつくるには、人工乳房を入れるだけの皮膚の余裕をつくらなければなりません。そこで行われるのが、エキスパンダーによる皮膚の拡張です。 簡単にいえば、皮膚を伸ばす器具を胸に入れて、ゆっくりと時間をかけて皮膚を伸ばしていくのです。そのあと、人工乳房を挿入します。なおエキスパンダーという拡張器を使った1次再建の利点として、エキスパンダーを入れてから、人工乳房にするか、皮弁形成術にするか考える時間があること、またエキスパンダーを入れた後で切除断端陽性、放射線照射が必要などの問題があっても、エキスパンダーはどうしてもやむをえない場合は、局所麻酔で日帰り手術で容易に抜去できるので、自家組織による一次再建のような大きな問題にならないことが利点です。 二次再建で行う場合は、乳房切除術が終わって傷が治ったところで、エキスパンダーを埋め込む手術をします。乳房を切除したときの傷口を利用してメスを入れ、大胸筋をはがし、その下にエキスパンダーを埋め込みます。1時間程度の手術です。 エキスパンダーは袋になっているので、最初はここに少量の生理食塩水を入れます。あとは、週に一度から月に一度の割合で、生理食塩水の量を増やして皮膚を伸ばしていきます。反対側の乳房よりやや大きめのふくらみになったところで、生理食塩水の増量はストップします。そして、そのままの状態を3カ月ほど維持します。エキスパンダーを取り除いても皮膚が元に戻らないように十分に皮膚を伸ばすためです。 ここで、十分皮膚が伸びていれば、乳房もやわらかく自然な形にできます。その後、また手術でエキスパンダーを除去し、かわりにシリコンの人工乳房を挿入します。乳頭部や乳輪は、そのあとで再建します。 最初にエキスパンダーをちょうどいい位置に挿入し、皮膚を上手に伸ばすのがこの再建法のポイントです。
【人工乳房再建の長所と短所】
人工乳房を使った再建術は、体への負担か少ないのが利点です。2回手術をするといっても、両方とも1回目は1時間、2回目は30分程度の短い手術です。入院も数日以内です。 また人工乳房の利点はやり直しがきくことです。後で人工乳房を除去して皮弁での再建をやり直すことはできますが、その逆はできません。局所再発した場合にも人工乳房なら除去して再発治療を行い、後で再度乳房再建を行うことができるというのも大きなメリットです。 短所は、エキスパンダーで皮膚を拡張するときに、皮膚が破れたりゆがんで伸びてしまうこともあります。また、反対側の乳房は年齢とともに下垂してきますが、人工乳房を埋め込んだ乳房はいつまでも若々しく、張りがあります。その調整のために再手術が必要になることもあります。
インプラント手術例一覧
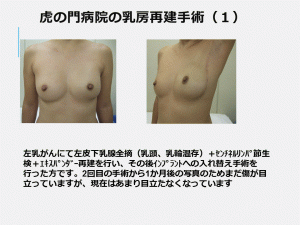
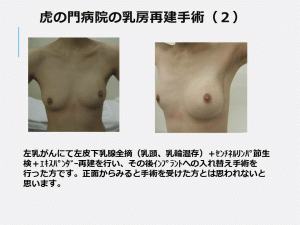
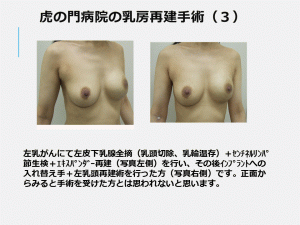
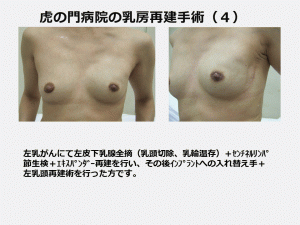
術後7年経過の例(アクセス制限あり)
ログイン情報はこちらへお問い合わせください
自家組織による再建
定型的手術(ハルステッド法)などで、乳房といっしょに大胸筋まで切除した場合は、人工乳房だけで乳房を再建することは困難です。過去にこの手術を受けた方の場合には、自家組織による乳房再建が唯一の選択肢になります。しかし現在の乳がん手術は大胸筋温存が原則のため、自家組織による再建と、人工乳房による再建の2つの選択肢があります。どちらが適しているかは、患者さんの元々の体型とがんの手術内容が決め手となります。
自家組織による再建は、患者さん自身の体の一部を使って乳房を再建する方法です。 実際には、腹部の組織を使う「腹直筋皮弁(ふくちょくきんひべん)法」と、背中の組織を使う「広背筋皮弁(こうはいきんひべん)法」があります。ここでは有茎皮弁法と呼ばれる、皮膚、脂肪、筋肉に血管をつけたまま別の部位に移植する方法について説明します。
【広背筋皮弁法】
広背筋は、腕のつけ根から背中や腰の方に向かって扇型に広がる筋肉です。この筋肉に皮膚と脂肪をつけたままはがし、血管は温存したまま、切除した乳房部に移植します。背中の筋肉は比較的薄くて脂肪も少ないので、乳房のボリュームが出にくい欠点があります。この方法は比較的負担の少ないいい方法ですが、患者さんの体型によっては不向きなこともあります。
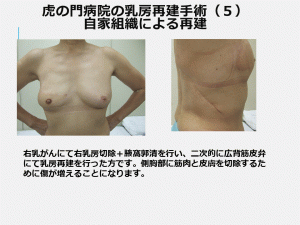
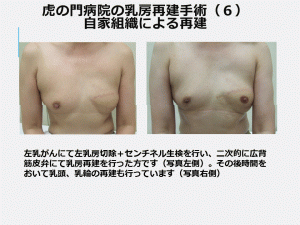
【腹直筋皮弁法】
腹部には、中心部をタテに走る太い腹直筋が2本あります。腹部には脂肪も多く、広背筋よりボリュームが出せるのが利点です。 このうちどちらか一つの筋肉に脂肪と皮膚をつけて、さらに血管をつけたまま切除した乳房部に移植します。 腹直筋でつくった乳房は柔らかく、本物の乳房とよく似た感触があります。
【自家移植の長所と短所】
自家移植は、異物を使わないことと、やわらかいぬくもりがあるのが利点です。しかし、乳房と、組織を取ってきた背中や腹部に傷が残るのが欠点です。きれいに縫って、下着に隠れるような位置にしてありますが、傷が消えることはありません。手術自体も、人工乳房にくらべれば大きくなり、入院期間も1~2週間は必要です。 特に、腹直筋を使った手術は体への負担が大きく、元の生活に戻るためには、2~3カ月かかると思っていてください。また、腹筋が弱くなるので、これから妊娠出産を考えている人には適応できない方法です。
【遊離皮弁法】
筋皮弁を完全に遊離して血管吻合する方法もあります。デザインの自由度が増し、仕上がりが最も期待できる方法です。反面、血管吻合がうまくいかないと遊離した組織が生着しないという大きなリスクを伴います。 人工乳房の場合は、以前は周囲に線維化が起き、固く変形する(被膜拘縮)ことも少なくありませんでしたが、今でも素材がよくなりトラブルの頻度は少なくなりました。それでもこうしたトラブルがないわけではなく人工乳房を除去しなくてはならないこともあり得ます。自家組織でも、まれに組織が生着しなかったり、血流がうまく流れなくて組織が死んでしまうことがあり得るなど、医療には絶対はないため、こうしたリスクを十分理解して手術に臨まれることが必要でしょう。
【乳頭部と乳輪の再建】
乳房再建の仕上げが、乳頭部と乳輪の再建です。これは、乳房再建による乳房のふくらみが落ちついたあとで、ゆっくり行います。3か月から1年ぐらいたってからと考えて下さい。 乳頭部と乳輪の再建にも、いくつかの方法があります。もし乳頭部がわりあい大きい人ならば、反対側の乳頭部と乳輪を半分切って移植することもできます。反対側の乳房から取ってくるので、色も性質も自然なのが利点です。ただ、健康なほうの乳房にもメスを入れるのが難点です。手術は1時間ほどで、傷もやがてわからなくなりますが、授乳はできなくなります。 新たにつくる場合は、乳頭部にあたる部分の皮膚を立体的に盛り上げ、乳輪はTattooで皮膚を染めてつくります。乳頭部の再建には保険が効きますが、Tattooによる乳輪の再建は現時点では保険が効きません。 乳房再建に関する保険適応の問題、費用の問題はやや複雑です。またトラブルが起きた時、費用を誰が負担するのかという問題もあります。このため事前によく費用の問題を確認しておくことが重要です。
乳頭部と乳輪の再建例(アクセス制限あり)
ログイン情報はこちらへお問い合わせください
[コラム] 放射線と乳房再建
放射線照射をすると、皮膚が萎縮(いしゅく)したり、人工乳房に皮膜ができて固く拘縮(こうしゆく)するおそれがあるので、照射前に乳房再建は行わないのがふつうです。放射線治療後は、皮膚のダメージの具合によります。エキスパンダーを使っても皮膚が伸びないこともあるので、自家組織を使うのが原則です。しかし、いろいろな工夫もあるので、乳房再建の専門家に相談してみましょう。
乳房全摘手術後に乳房再建手術を行った例(アクセス制限あり)
ログイン情報はこちらへお問い合わせください
